题目内容
阿斯匹林(aspirin)的有效成分是乙酰水杨酸,它是19世纪末合成成功的,作为一个有效的解热止痛、治疗感冒的药物,至今仍广泛使用,有关报道表明,人们正在发现它的某些新功能。阿斯匹林是由水杨酸(邻羟基苯甲酸)与乙酸酐进行酯化反应而得的。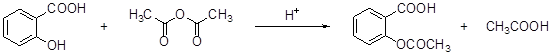
水杨酸 乙酸酐 乙酰水杨酸
(1)乙酰水杨酸的含氧官能团分别是 和酯基。
(2)乙酰水杨酸不应具有的性质( )
| A.与NaOH溶液反应 | B.与金属钠反应 |
| C.与乙酸发生酯化反应 | D.与乙醇发生酯化反应 |
(4)为测定阿斯匹林中有效成分的含量,称取样品0.250 0 g ,准确加入浓度为0.1015 mol·L- NaOH溶液50.00 mL,煮沸60min。冷却后用浓度为0.1015 mol·L-1的HC1溶液返滴过量的NaOH,消耗HC1溶液记录如下:
| 次数 数据 | 1 | 2 | 3 |
| 初始读数 | 2.00 | 12.50 | 5.20 |
| 最后读数 | 27.10 | 37.40 | 33.20 |
(1)羧基 (2)C (3)略
(4)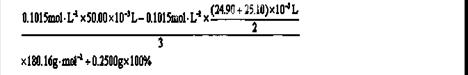
解析试题分析:(1)由乙酰水杨酸的结构简式知其含氧官能团为羧基和酯基;(2)乙酰水杨酸中含有羧基和酯基,二者都能与NaOH溶液反应,羧基能与金属钠反应、与乙醇发生酯化反应,选C;(3)乙酰水杨酸中含有酯基,酸性条件下发生水解反应生成酸和醇(或酚),可得方程式;(4)根据阿司匹林的结构可知:1mol阿司匹林能与3molNaOH反应,消耗HCl的体积有1、2两组数据计算,第3组数据相差较大,舍弃。根据题意可列计算式: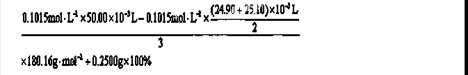
考点:考查有机物的结构和性质,酸碱中和滴定的计算。

练习册系列答案
相关题目
某烃类化合物A的用仪器可以测出其相对分子质量为84,分子中含有碳碳双键,分子中只有一种类型的氢。
(1)现有以下的实验室仪器:
| A.1H核磁共振仪 | B.质谱仪 | C.红外光谱仪 | D.元素分析仪 |
②测出官能团碳碳双键 、③测出几种类型的氢 。
(2)结合题给信息,可以判断A的结构简式为 ;
A中的的碳原子是以什么形式杂化? ;
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
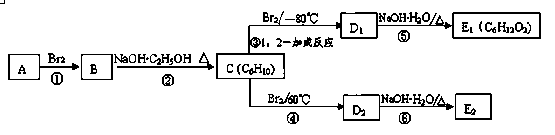
反应②的化学方程式为 ;
C的名称为 ;反应类型为 ;。
E2的结构简式是 ;④、⑤的反应类型依次是

 、
、 A、B、C三种有机物的分子式均为C3H6O2,分子中都含有甲基。做有关实验并记录反应情况如下表:
| | NaOH溶液 | 银氨溶液,加热 | 新制Cu(OH)2 | 金属钠 |
| A | 中和反应 | 无银镜 | 溶解 | 产生氢气 |
| B | 不反应 | 有银镜 | 加热,有红色沉淀 | 产生氢气 |
| C | 水解反应 | 有银镜 | 加热,有红色沉淀 | 不反应 |
则A、B、C三种有机物的结构简式分别为:
A_______________________,B_________________________,C_______________________________。
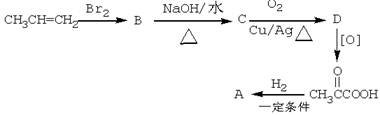
 : 反应类型:
: 反应类型:  : 反应类型: ;
: 反应类型: ;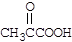 在一定条件下容易发生“脱羧”反应,产物之一为甲醛的同系物,写出该产物的结构简式: 。
在一定条件下容易发生“脱羧”反应,产物之一为甲醛的同系物,写出该产物的结构简式: 。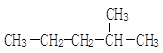 的系统命名是:
的系统命名是: 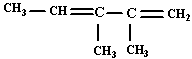 的系统命名是
的系统命名是 


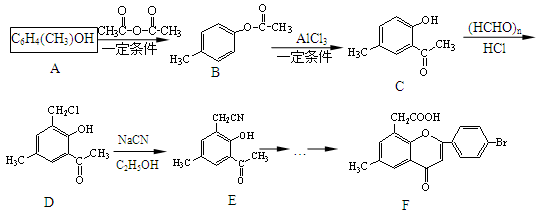
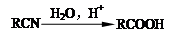
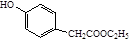 )是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。
)是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。