��Ŀ����
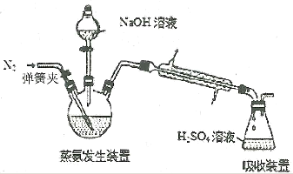
����Ŀ�����Ṥҵβ���е�NO��NO2����������γɹ⻯ѧ�������ƻ�������ȡ���������������Һ�Ժ����������β�����д�������Ӧ�Ļ�ѧ����ʽ���£�NO2+NO+2NaOH=2NaNO2+H2O��2NO2+2NaOH=NaNO2+NaNO3+H2O������Ҳ����������������������磬������һ�������ɷ������·�Ӧ��4NH3+6NO=5N2+6H2O����һ����NO��NO2�Ļ������ͨ��300mL5mol/LNaOH��Һ�У�ǡ�ñ���ȫ���ա�����˵������ȷ����
A.���ð���������������ʱ�������������ԭ��Ӧ
B.������Һ��NaNO3��NaNO2�����ʵ���֮�ȿ���Ϊ2��1
C.���ð������������谱���ڱ�״���µ��������Ϊ39.2L
D.ԭ���������NO�ڱ�״���µ��������Ϊ16.8L
���𰸡�B
��������
A.���ð���������������ʱ�����������õ��ӣ�Ԫ�ػ��ϼ۽��ͣ�������ԭ��Ӧ��A��ȷ��
B.��ֻ������Ӧ2NO2+2NaOH=NaNO2+NaNO3+H2O����Ӧ������n(NaNO3)��n(NaNO2)=1��1����ͬʱ��������ӦNO2+NO+2NaOH=2NaNO2+H2O������Һ��n(NaNO2)>n(NaNO3)��������Һ��NaNO3��NaNO2�����ʵ���֮�Ȳ�����Ϊ2��1��B����
C.300 mL 5mol/LNaOH��Һ��n(NaOH)=0.3L��5mol/L=1.5mol��NO��NO2��NaOH��Һ��Ӧ������NaNO3��NaNO2������Ԫ���غ��֪n(NO)+n(NO2)=1.5mol����ֻ����NO2+NO+2NaOH=2NaNO2+H2O��n(NO)=0.75mol��n(NO2)=0.75mol����Ӧ4NH3+6NO=5N2+6H2O����NH3�����ʵ���Ϊn(NH3)=![]() ��0.75mol����Ӧ8NH3+6NO2=7N2+12H2O����NH3�����ʵ���Ϊn(NH3)=
��0.75mol����Ӧ8NH3+6NO2=7N2+12H2O����NH3�����ʵ���Ϊn(NH3)=![]() ��0.75mol����Ӧ������NH3�����ʵ���Ϊ
��0.75mol����Ӧ������NH3�����ʵ���Ϊ![]() ��0.75mol+
��0.75mol+![]() ��0.75mol=1.5mol�������ΪV(NH3)=1.5mol��22.4L/mol=33.6L��������ֻ��NO2�������8NH3+6NO2=7N2+12H2O��֪������NH3�����ʵ���Ϊn(NH3)=
��0.75mol=1.5mol�������ΪV(NH3)=1.5mol��22.4L/mol=33.6L��������ֻ��NO2�������8NH3+6NO2=7N2+12H2O��֪������NH3�����ʵ���Ϊn(NH3)=![]() ��1.5mol=2mol�������ΪV(NH3)=2.0mol��22.4L/mol=44.8L���ڻ�����������������n(NO2)��n(NO)>1��1�����Է�Ӧ���İ������������33.6L��44.8L֮�䣬����Ϊ39.2L��C��ȷ��
��1.5mol=2mol�������ΪV(NH3)=2.0mol��22.4L/mol=44.8L���ڻ�����������������n(NO2)��n(NO)>1��1�����Է�Ӧ���İ������������33.6L��44.8L֮�䣬����Ϊ39.2L��C��ȷ��
D.300 mL 5mol/LNaOH��Һ��n(NaOH)=0.3L��5mol/L=1.5mol����ֻ����NO2+NO+2NaOH�T2NaNO2+H2O��n(NO)=0.75mol�����ڱ�״�����������V(NO)=22.4L/mol��0.75mol=16.8L��D��ȷ��
�ʴ�ѡB��

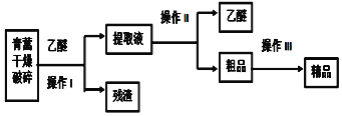
����Ŀ����֪��ˮ��ȡþ����Ҫ�������£�
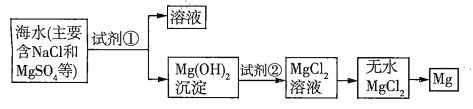
(1)���ڼ����Լ������������������·�����������������⡣
���� | �Ƿ���� | �������� |
���������¼���������ˮ���ټ�������� | a | b |
��������������������c |
a. _____________��
b.____________��
c.____________��
(2)��ͼ�м�����Լ���Ӧ����_______(����������)�������Լ��ڵ�������_______(�ѧʽ)����ҵ������ˮ![]() ��ȡþ�Ļ�ѧ����ʽΪ___________��
��ȡþ�Ļ�ѧ����ʽΪ___________��
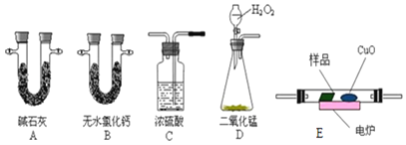
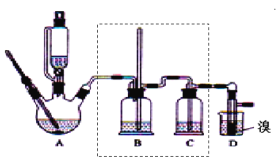
����Ŀ��ʵ�����Ʊ�1��2���������飬�����������Ҵ����Ʊ���ϩ��������ϩ�����������Ʊ�1��2���������飬װ����ͼ��ʾ���й������б������ʾ���ش��������⣺
�Ҵ� | 1��2���������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/gcm-3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | -130 | 9 | -116 |
��1���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ����__��
a.������Ӧ b.�ӿ췴Ӧ�ٶ�
c.��ֹ�Ҵ��ӷ� d.���ٸ�������������
��2����װ��A�г���Ũ������Ҵ��⣬��Ӧ����__����Ŀ����__��װ��A�����ɸ��������ѵĻ�ѧ��Ӧ����ʽΪ__��
��3��ʵ������ȡ��ϩ�������¶ȹ��߶�ʹ�Ҵ���ŨH2SO4��Ӧ����������SO2��Ϊ����֤SO2�Ĵ��ڲ���ȥSO2�Ժ�����Ӧ�ĸ��ţ�ijͬѧ��A��D֮�������B��C����װ�ã�����B��C�пɷֱ�ʢ��___��
a.����KMnO4��ˮ b.Ʒ���NaOH��Һ
c.����KMnO4��NaOH��Һ d.Ʒ�������KMnO4
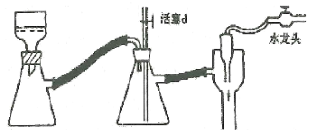
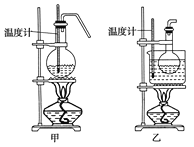
��4���ס�����װ�þ�������ʵ��������ˮ�Ҵ���ȡ��ϩ����ͼ���ø���ԡ����(���ͷе�290�棬�۵�18.17��)���������¶ȴﵽ��Ӧ�¶�ʱ����ʢ����ˮ�Ҵ���Ũ������Һ����ƿ��������У��ܿ�ﵽ��Ӧ�¶ȡ��ס�����װ����Ƚϣ���װ������Щ�ŵ�__��д����ʵ��������ˮ�Ҵ���ȡ��ϩ�Ļ�ѧ����ʽ___��
��5����1��2����������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ú���Ӧ��__�㣻�����������������������ѡ�����__�ķ�����ȥ��