��Ŀ����
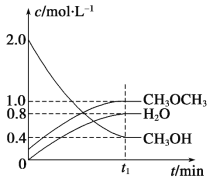
����Ŀ��2SO2��g��+O2��g��=2SO3��g����Ӧ���̵������仯��ͼ��ʾ��
��֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H=��99kJmol��1 �� ��ش��������⣺
��1��ͼ��A��C�ֱ��ʾ��
��2��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ������Ӱ�죿 �� �÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�������ǽ��ͣ� �� ������
��3��ͼ�С�H=KJmol��1 ��
���𰸡�
��1����Ӧ������,����������
��2����,����,��Ϊ�����ı��˷�Ӧ������ʹ���E����
��3����198
���������⣺��1����ͼ��A��C�ֱ��ʾ��Ӧ������������������������
���Դ��ǣ���Ӧ��������������������
��2��EΪ��ܣ���Ӧ�ȿɱ�ʾΪA��C��ܵĴ�С֮���ܵĴ�С�뷴Ӧ���أ���������ı��˷�Ӧ��;�������ͷ�Ӧ����Ļ�ܣ�����E�ı仯�Ǽ�С��
���Դ��ǣ��ޣ����ͣ���Ϊ�����ı��˷�Ӧ������ʹ���E���ͣ�
��3����1mol SO2��g������Ϊ1mol SO3�ġ�H=��99kJmol��1������2molSO2��g������Ϊ2molSO3�ġ�H=��198kJmol��1����2SO2��g��+O2��g��=2SO3��g����H=��198KJmol��1��
���Դ��ǣ���198��
�����㾫�������շ�Ӧ�Ⱥ��ʱ��ǽ����ĸ�������Ҫ֪���ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�