题目内容
2.下列离子方程式书写正确的是( )| A. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性,2MnO4-+6H++5 H2O2=2Mn2++5O2↑+8H2O | |
| B. | 硅与氢氧化钠溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ | |
| C. | 次氯酸钠溶液中通入过量的SO2气体:ClO-+SO2+H2O═HClO+HSO3- | |
| D. | 足量硫化氢气体通入硫酸铁溶液中:H2S+Fe3+=Fe2++S↓+2H+ |
分析 A.浓盐酸可以被酸性高锰酸钾溶液氧化;
B.反应生成硅酸钠和氢气;
C.反应生成硫酸钠和氯化钠;
D.电子、电荷不守恒.
解答 解:A.浓盐酸可以被酸性高锰酸钾溶液氧化,从而影响双氧水还原性的检验,故A错误;
B.硅与氢氧化钠溶液反应的离子反应为Si+2OH-+H2O═SiO32-+2H2↑,故B正确;
C.次氯酸钠溶液中通入过量的SO2气体的离子反应为ClO-+H2O+SO2═SO42-+2H++Cl-,故C错误;
D.足量硫化氢气体通入硫酸铁溶液中的离子反应为H2S+2Fe3+═2Fe2++S↓+2H+,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案
相关题目
12.能正确表示下列化学反应的离子方程式的是( )
| A. | 澄清的石灰水与稀盐酸反应:OH-+H+=H2O | |
| B. | 氢氧化钡溶液与稀硫酸反应:Ba2++OH-+SO${\;}_{4}^{2-}$+H+=BaSO4↓+H2O | |
| C. | 氧化铜与盐酸反应:O2-+2H+=H2O | |
| D. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
13.下列关于胶体的说法正确的是( )
| A. | 胶体与溶液有明显不同的外观特征,胶体呈胶状 | |
| B. | 胶体不稳定,静置后容易产生沉淀 | |
| C. | 将Fe(OH)3胶体进行过滤,所得滤液与原来胶体组成是不同的 | |
| D. | 豆浆是胶体,因为豆浆中的分散质粒子直径介于1nm-100nm之间 |
10.区别植物油和矿物油的正确方法是( )
| A. | 加水振荡,观察是否有分层现象 | |
| B. | 加乙醇振荡,观察是否发生分层 | |
| C. | 加新制Cu(OH)2悬浊液,煮沸,观察有无砖红色沉淀生成 | |
| D. | 加入含有酚酞的NaOH溶液,加热,观察红色是否变浅 |
17.若用乙烯和氯气在适当的条件下反应制取四氯乙烷,这一过程中所要经历的反应及耗用氯气的量是(设乙烯为1mol,反应产物中的有机物只是四氯乙烷)( )
| A. | 取代,4 mol Cl2 | B. | 加成,2 mol Cl2 | ||
| C. | 加成、取代,2 mol Cl2 | D. | 加成、取代,3 mol Cl2 |
7.下列四个选项的描述正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | CH3C(CH3)2CH2CH2CH(CH2CH3)CH3 的系统命名为:2,2,5-三甲基庚烷 | |
| C. | 羟基的电子式: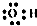 | |
| D. | CCl4的电子式: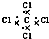 |
14.下列离子方程式正确的是( )
| A. | 澄清的石灰水与盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 钠与水的反应 Na+2H2O═Na++2OH-+H2↑ | |
| C. | 铜片插入硝酸银溶液 Cu+Ag+═Cu2++Ag | |
| D. | 大理石溶于醋酸 CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ |
11.短周期主族元素A、B、C、D的原子序数依次增大,A、B、C原子的最外层电子数之和为12,B、C、D位于同一周期,C原子的最外层电子数既是A原子内层电子数的3倍又是B原子最外层电子数的3倍.下列说法正确的是( )
| A. | 元素A、C的最高价氧化物对应的水化物都是弱酸 | |
| B. | D的单质有毒,且有漂白性,其氢化物比同主族其它元素氢化物的沸点更高 | |
| C. | 元素B和D能形成BD2型的共价化合物 | |
| D. | 元素B的单质能与A的最高价氧化物发生置换反应 |
 .
.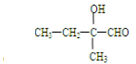 、
、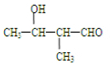 .
.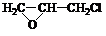 +nOHCH2CH2OH$\stackrel{一定条件}{→}$
+nOHCH2CH2OH$\stackrel{一定条件}{→}$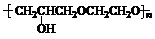 +nHCl
+nHCl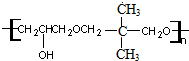 .
.