题目内容
14.下列离子方程式正确的是( )| A. | 澄清的石灰水与盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 钠与水的反应 Na+2H2O═Na++2OH-+H2↑ | |
| C. | 铜片插入硝酸银溶液 Cu+Ag+═Cu2++Ag | |
| D. | 大理石溶于醋酸 CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ |
分析 A.反应生成氯化钙和水;
B.电子、电荷不守恒;
C.电子、电荷不守恒;
D.反应生成醋酸钙、水、二氧化碳.
解答 解:A.澄清的石灰水与盐酸反应的离子反应为OH-+H+═H2O,故A错误;
B.钠与水的反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.铜片插入硝酸银溶液的离子反应为Cu+2Ag+═Cu2++2Ag,故C错误;
D.大理石溶于醋酸的离子反应为CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目
4.化学与人类生活、工农业生产、科学技术等息息相关,下列说法正确的是( )
| A. | 在涂料中尽量用液态有机物代替水作溶剂以减少环境污染 | |
| B. | 世博会很多场馆的外壳使用非晶硅薄膜,以充分利用太阳能,体现低碳经济 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 绿色化学的核心是应用化学原理对环境污染进行治理 |
5.下列说法正确的是( )
| A. | 聚乙烯可发生加成反应 | |
| B. | 乙烯和甲烷可用酸性高锰酸钾溶液鉴别 | |
| C. | 乙烯和苯都能与溴水反应 | |
| D. | 乙烯和乙烷都能发生加成反应 |
2.下列离子方程式书写正确的是( )
| A. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性,2MnO4-+6H++5 H2O2=2Mn2++5O2↑+8H2O | |
| B. | 硅与氢氧化钠溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ | |
| C. | 次氯酸钠溶液中通入过量的SO2气体:ClO-+SO2+H2O═HClO+HSO3- | |
| D. | 足量硫化氢气体通入硫酸铁溶液中:H2S+Fe3+=Fe2++S↓+2H+ |
9.有关化学用语正确的是( )
| A. | 乙烯的实验式:C2H4 | B. | 乙炔的电子式: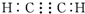 | ||
| C. | 甲酸甲酯的结构简式:C2H4O | D. | 氢氧根电子式: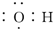 |
19.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | CO2→H2CO3 | B. | SiO2→Na2SiO3 | C. | SiO2→H2SiO3 | D. | Na2O2→Na2CO3 |
6.依据题目要求回答下列问题.
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合H+能力最强的是CO32-
②据上表数据,请你判断下列反应不能成立的是D(填编号)
A、CH3COOH+Na2CO3═NaHCO3+CH3COONa
B、CH3COOH+NaCN═CH4COONa+HCN
C、CO2+H2O+NaClO═NaHCO3+HClO
D、CO2+H2O+2C4H5ONa═Na2CO3+2C8H5OH
③要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为Cl2+HCO3-═CO2+Cl-+HClO.
(2)已知温下Cu(OH)2的Ksp=2×10-20,又知常温下某CuSO4溶液里c(Cu2+)=0.02mol•L-1.如果要生成Cu(OH)2,则应调整溶液pH大于5.
(3)已知可逆反应FeO(g)+CO(g)?Fe(g)+CO2(g)是炼铁工业中一个重要反应,某温度与平衡常数K的关系如下表:
①写出该反应平衡常数的表达式:K=$\frac{c(CO)}{c(C{O}_{2})}$.
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件:升高温度,混合气体的密度减小(选填“增大”“碱小”或“不变”):当$\frac{n(C{O}_{2})}{n(CO)}$=0.5,混合气体平均相对分子质量为33.3.
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C4H4ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②据上表数据,请你判断下列反应不能成立的是D(填编号)
A、CH3COOH+Na2CO3═NaHCO3+CH3COONa
B、CH3COOH+NaCN═CH4COONa+HCN
C、CO2+H2O+NaClO═NaHCO3+HClO
D、CO2+H2O+2C4H5ONa═Na2CO3+2C8H5OH
③要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为Cl2+HCO3-═CO2+Cl-+HClO.
(2)已知温下Cu(OH)2的Ksp=2×10-20,又知常温下某CuSO4溶液里c(Cu2+)=0.02mol•L-1.如果要生成Cu(OH)2,则应调整溶液pH大于5.
(3)已知可逆反应FeO(g)+CO(g)?Fe(g)+CO2(g)是炼铁工业中一个重要反应,某温度与平衡常数K的关系如下表:
| T(K) | 933 | 1100 |
| K | 0.68 | 0.40 |
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件:升高温度,混合气体的密度减小(选填“增大”“碱小”或“不变”):当$\frac{n(C{O}_{2})}{n(CO)}$=0.5,混合气体平均相对分子质量为33.3.
3.下列氢化物中,按稳定性由强到弱的顺序排列的是( )
| A. | HI、HBr、HCl、HF | B. | HCl、PH3、H2S、SiH4 | ||
| C. | H2O、H2S、HCl、HBr | D. | HF、H2O、NH3、CH4 |
4.某有机物的结构简式为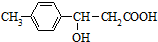 ,它可发生的有机反应的正确组合是( )
,它可发生的有机反应的正确组合是( )
①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
 ,它可发生的有机反应的正确组合是( )
,它可发生的有机反应的正确组合是( )①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
| A. | ①②③⑤⑥ | B. | ②③④⑥⑧ | C. | ①②③⑤⑥⑦ | D. | ④⑤⑥⑦⑧ |