题目内容
短周期主族元素A、B、C、D的原子序数依次增大,它们的原子核外电子层数之和为7。B的化合物种类繁多,数目庞大。A与D能形成原子个数比为1∶1和2∶1的化合物。(1)只由A、B、D组成的化合物中,相对分子质量最小的是_____________,写出该化合物的一种用途______________,人类六大营养素中,只由A、B、D三种元素组成的有______________(填其中一种营养素的名称)。
(2)只由A、C组成的一种常见气态化合物,其电子式为______________,工业上合成该气体的化学方程式为________________________________________________。往等体积的Ⅰ、Ⅱ两个密闭容器中分别充入1 mol A单质和1 mol C单质、2 mol A单质和2 mol C单质。一定条件下,充分反应后分别达到平衡(两容器温度相等)。正确表示Ⅰ、Ⅱ容器中A单质的物质的量分数(φ)随时间(t)变化的示意图是______________(填标号)。

(3)只由A、C、D组成的盐,发生水解反应的离子方程式为_______________________。
(4)甲、乙两种化合物都只由A、B、C、D四种元素组成,它们既能与盐酸反应又能与烧碱溶液反应。其中,甲为无机酸式盐,甲与稀烧碱溶液反应的离子方程式是____________;乙为天然蛋白质水解的相对分子质量最小的产物,其结构简式为_____________________。
(1)HCHO(或 ![]() 、甲醛)
、甲醛)
作消毒剂(或作防腐剂、作化工原料等合理答案)
糖类(或油脂)
(2)![]() N2+3H2
N2+3H2![]() 2NH
2NH
(3)![]() +H2O
+H2O![]() NH3·H2O+H+(若其他合理答案也可)
NH3·H2O+H+(若其他合理答案也可)
(4)![]() +
+![]() +2OH-====NH3·H2O+H2O+
+2OH-====NH3·H2O+H2O+![]()
![]()
解析:由题知B为C,A为H,D为O,那么C只能为N。
(1)由C、H、O组成的化合物且相对分子质量最小的是甲醛。
(2)该气态化合物为NH3,工业上合成NH3的化学方程式为N2+3H2![]() 2NH3。等体积时,Ⅱ中A、C物质的量浓度是Ⅰ中的2倍,故反应速率快达到平衡所需时间短,对Ⅱ中2 mol A和2mol C进行如下处理,先加1 mol A和1 mol C,待平衡后再加入1 mol A和1 mol C,在恒温恒容时,相当于加压,平衡向正反应方向移动,Ⅱ中A的转化率比Ⅰ中大,则平衡时混合物中Ⅱ的A%比Ⅰ的低。
2NH3。等体积时,Ⅱ中A、C物质的量浓度是Ⅰ中的2倍,故反应速率快达到平衡所需时间短,对Ⅱ中2 mol A和2mol C进行如下处理,先加1 mol A和1 mol C,待平衡后再加入1 mol A和1 mol C,在恒温恒容时,相当于加压,平衡向正反应方向移动,Ⅱ中A的转化率比Ⅰ中大,则平衡时混合物中Ⅱ的A%比Ⅰ的低。
(3)由O、H、N组成的盐为NH4NO3,故![]() 水解而使溶液显酸性。
水解而使溶液显酸性。
(4)由H、C、O、N形成两种化合物,既能与盐酸反应又能与烧碱反应。若为无机酸式盐,应为NH4HCO3;若为天然蛋白质水解产物即氨基酸,那么分子量最小的氨基酸是甘氨酸。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A、原子半径:A<D<C<B | B、B、C、D分别与A形成的化合物一定含有相同的化学键 | C、最高价氧化物对应水化物的酸性:D<C | D、常温下,单质B能大量溶于浓硝酸中 |
| A、原于半径A<B<C | B、A的气态氢化物稳定性大于C的气态氢化物稳定性 | C、A、C两元素最高价氧化物均可与水化合得到对应的酸 | D、高温时,A单质可以从C的氧化物中置换得到C单质 |
| A、原子半径由小到大的顺序:r(C)<r(D)<r(E) | B、元素D、E分别与A形成的化合物的热稳定性:E>D | C、元素D的最高价氧化物对应水化物的酸性比E的强 | D、元素B分别与A、C形成的化合物中化学键的类型完全相同 |
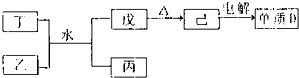
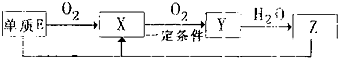
 短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物.
短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物. NH3?H2O+H+
NH3?H2O+H+ 2NO2
2NO2