МвДїДЪИЭ
ЎѕМвДїЎї№¤ТµЙПТФёхМъїу(ЦчТЄіЙ·ЦОЄFeOЎ¤Cr2O3)ЎўМјЛбДЖЎўСхЖшєНБтЛбОЄФБПЙъІъЦШёхЛбДЖ(Na2Cr2O7Ў¤2H2O)Ј¬ЖдЦчТЄ·ґУ¦ОЄўЩ4FeOЎ¤Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2Ј¬ўЪ2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2OЈ¬ПВБРЛµ·ЁХэИ·µДКЗ (ЎЎЎЎ)
8Na2CrO4+2Fe2O3+8CO2Ј¬ўЪ2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2OЈ¬ПВБРЛµ·ЁХэИ·µДКЗ (ЎЎЎЎ)
A. ·ґУ¦ўЩєНўЪѕщОЄСх»Ї»№Ф·ґУ¦
B. ·ґУ¦ўЩµДСх»ЇјБКЗO2Ј¬»№ФјБКЗFeOЎ¤Cr2O3
C. ёЯОВПВЈ¬O2µДСх»ЇРФЗїУЪFe2O3Ј¬ИхУЪNa2CrO4
D. ·ґУ¦ўЩЦРГїЙъіЙ1 mol Na2CrO4К±ЧЄТЖµзЧУ3 mol
Ўѕґр°ёЎїB
ЎѕЅвОцЎї
A. 4FeOЎ¤Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2ЦРУРФЄЛШ»ЇєПјЫµД±д»ЇЈ¬ЛщТФКЗСх»Ї»№Ф·ґУ¦Ј¬¶ш2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2OЦРГ»УРФЄЛШ»ЇєПјЫµД±д»ЇЈ¬ЛщТФІ»КЗСх»Ї»№Ф·ґУ¦Ј¬№КAґнОуЈ»
8Na2CrO4+2Fe2O3+8CO2ЦРУРФЄЛШ»ЇєПјЫµД±д»ЇЈ¬ЛщТФКЗСх»Ї»№Ф·ґУ¦Ј¬¶ш2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2OЦРГ»УРФЄЛШ»ЇєПјЫµД±д»ЇЈ¬ЛщТФІ»КЗСх»Ї»№Ф·ґУ¦Ј¬№КAґнОуЈ»
B. 4FeOЎ¤Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2ЦРЈ¬СхЖшЦРСхФЄЛШµГµзЧУ»ЇєПјЫЅµµНЈ¬ЛщТФСх»ЇјБКЗСхЖшЈ¬МъФЄЛШєНёхФЄЛШК§µзЧУ»ЇєПјЫЙэёЯЈ¬ЛщТФ»№ФјБКЗFeOЎ¤Cr2O3Ј¬№КBХэИ·Ј»
8Na2CrO4+2Fe2O3+8CO2ЦРЈ¬СхЖшЦРСхФЄЛШµГµзЧУ»ЇєПјЫЅµµНЈ¬ЛщТФСх»ЇјБКЗСхЖшЈ¬МъФЄЛШєНёхФЄЛШК§µзЧУ»ЇєПјЫЙэёЯЈ¬ЛщТФ»№ФјБКЗFeOЎ¤Cr2O3Ј¬№КBХэИ·Ј»
C. 4FeOЎ¤Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2ЦРЦРЈ¬Сх»ЇјБКЗСхЖшЈ¬»№ФјБКЗFeOЎ¤Cr2O3Ј¬ЛщТФСхЖшµДСх»ЇРФґуУЪNa2CrO4єНFe2O3Ј¬µ«І»ДЬЕР¶ПNa2CrO4єНFe2O3µДСх»ЇРФПа¶ФЗїИхЈ¬№КCґнОуЈ»
8Na2CrO4+2Fe2O3+8CO2ЦРЦРЈ¬Сх»ЇјБКЗСхЖшЈ¬»№ФјБКЗFeOЎ¤Cr2O3Ј¬ЛщТФСхЖшµДСх»ЇРФґуУЪNa2CrO4єНFe2O3Ј¬µ«І»ДЬЕР¶ПNa2CrO4єНFe2O3µДСх»ЇРФПа¶ФЗїИхЈ¬№КCґнОуЈ»
D. УЙ·ЅіМКЅ4FeOЎ¤Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2 ЧЄТЖµзЧУїЙЦЄЈ¬ЙъіЙ1 mol Na2CrO4К±Ј¬ІОјУ·ґУ¦µДO2µДОпЦКµДБїОЄ
8Na2CrO4+2Fe2O3+8CO2 ЧЄТЖµзЧУїЙЦЄЈ¬ЙъіЙ1 mol Na2CrO4К±Ј¬ІОјУ·ґУ¦µДO2µДОпЦКµДБїОЄ![]() Ј¬·ґУ¦ЦРOФЄЛШУЙ0јЫЅµµНОЄ-2јЫЈ¬µзЧУЧЄТЖµДОпЦКµДБїОЄІОјУ·ґУ¦µДСхЖшµДОпЦКµДБїµД4±¶Ј¬ЧЄТЖµзЧУµДОпЦКµДБїОЄ
Ј¬·ґУ¦ЦРOФЄЛШУЙ0јЫЅµµНОЄ-2јЫЈ¬µзЧУЧЄТЖµДОпЦКµДБїОЄІОјУ·ґУ¦µДСхЖшµДОпЦКµДБїµД4±¶Ј¬ЧЄТЖµзЧУµДОпЦКµДБїОЄ![]() Ј¬ЛщТФ·ґУ¦ўЩЦРГїЙъіЙ1 mol Na2CrO4К±µзЧУЧЄТЖ
Ј¬ЛщТФ·ґУ¦ўЩЦРГїЙъіЙ1 mol Na2CrO4К±µзЧУЧЄТЖ![]() Ј¬№КDґнОуЎЈ
Ј¬№КDґнОуЎЈ
ґр°ёСЎBЎЈ

ЎѕМвДїЎїпШЈЁ31GaЈ©ЎўХаЈЁ32GeЈ©¶јКЗЦШТЄµДПЎУРЅрКфЈ¬ФЪ»ЇС§ґЯ»ЇјБЎў°лµјМеІДБПЎўРВДЬФґµИБмУтУ¦УГ№г·єЈ¬їЙґУХаГєИјЙХєуµД·ЫГє»ТЈЁє¬ Ga2O3ЎўGeO2ЎўSiO2ЎўAl2O3Ј©ЦРМбИЎЈ¬ Ії·ЦБчіМИзПВЈє

ТСЦЄЈє
ОпЦК | GaCl3 | GeCl4 | AlCl3 |
·Рµг/Ўж | 201 | 84 | 183ЈЁЙэ»ЄЈ© |
ЈЁ1Ј©ВЛФьµДЦчТЄіЙ·ЦОЄ_____ЎЈ
ЈЁ2Ј©ўЩЦР·ўЙъµД·ґУ¦УР Al2O3+6H+=2Al3++3H2OЎўGa2O3+6H+=2Ga3++3H2O єН_____ЎЈ
ЈЁ3Ј©ІЩЧч a µДГыіЖКЗ_____Ј¬ўЪЦРїШЦЖОВ¶ИµД·¶О§КЗ_____ЈЁМоЧЦДёРтєЕЈ©ЎЈ
aЈ®20~84Ўж bЈ®84~183Ўж cЈ®84~201Ўж
ЈЁ4Ј©ўЬЦР·ўЙъ·ґУ¦µД»ЇС§·ЅіМКЅКЗ__________________________________________ЎЈ
ЈЁ5Ј©пШДЬУл·РЛ®ѕзБТ·ґУ¦ЙъіЙЗвЖшЈ¬ХаФЪјУИИМхјюПВУлСОЛб»тПЎБтЛбІ»·ґУ¦ЎЈґУФЧУЅб№№ЅЗ¶ИЅвКНЖдФТтЈє______________________
ЈЁ6Ј©УГЕЁСОЛбЛб»ЇµДБЧЛбИэ¶ЎхҐЈЁTBPЈ©їЙТФґУІРТєЦРЭНИЎ Ga3+Ј¬Па№Ш·ґУ¦ОЄЈєTBP+GaCl3+HCl![]() TBPH+Ў¤GaCl
TBPH+Ў¤GaCl![]() ЎЈУГПЎ NaOH ИЬТє¶ФУР»ъПаЅшРР·ґЭНИЎЈ¬УГСОЛбµчЅЪ·ґЭНИЎТє pH ЦБ 5~6Ј¬И»єуЙэОВЦБ 85~95ЎжЛ®ЅвµГµЅ Ga(OH)3Ј¬ѕєуРшґ¦АнµГµЅґЦпШЎЈЅбєП»ЇС§УГУпЅвКНУГПЎ NaOH ИЬТє¶ФУР»ъПаЅшРР·ґЭНИЎµДФТтЈє_________________ЎЈ
ЎЈУГПЎ NaOH ИЬТє¶ФУР»ъПаЅшРР·ґЭНИЎЈ¬УГСОЛбµчЅЪ·ґЭНИЎТє pH ЦБ 5~6Ј¬И»єуЙэОВЦБ 85~95ЎжЛ®ЅвµГµЅ Ga(OH)3Ј¬ѕєуРшґ¦АнµГµЅґЦпШЎЈЅбєП»ЇС§УГУпЅвКНУГПЎ NaOH ИЬТє¶ФУР»ъПаЅшРР·ґЭНИЎµДФТтЈє_________________ЎЈ
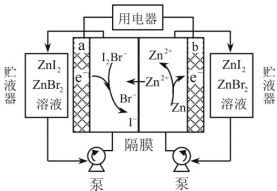
ЈЁ7Ј©µзЅв·ЁїЙТФМбґїґЦпШЈ¬ѕЯМеФАнИзНјЛщКѕЎЈпШФЪСфј«ИЬЅвЙъіЙµД Ga3+Ул NaOH ИЬТє·ґУ¦ЙъіЙ GaO![]() Ј¬GaO
Ј¬GaO![]() ФЪТхј«·ЕµзµДµзј«·ґУ¦КЅКЗ_____________________ЎЈ
ФЪТхј«·ЕµзµДµзј«·ґУ¦КЅКЗ_____________________ЎЈ
ЎѕМвДїЎїФЪТ»¶ЁМе»эµДГЬ±ХИЭЖчЦРЅшРРИзПВ»ЇС§·ґУ¦ЈєCO2(g)Ј«H2(g)![]() CO(g)Ј«H2O(g)Ј¬Жд»ЇС§ЖЅєвіЈКэ(K)єНОВ¶И(t)µД№ШПµИзПВ±нЛщКѕЈє
CO(g)Ј«H2O(g)Ј¬Жд»ЇС§ЖЅєвіЈКэ(K)єНОВ¶И(t)µД№ШПµИзПВ±нЛщКѕЈє
t/Ўж | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
»ШґрПВБРОКМвЈє
(1)ёГ·ґУ¦µД»ЇС§ЖЅєвіЈКэ±нґпКЅОЄKЈЅ_________________________ЎЈ
(2)ёГ·ґУ¦ОЄ____________(МоЎ°ОьИИЎ±»тЎ°·ЕИИЎ±)·ґУ¦ЎЈ
(3)ДЬЕР¶ПёГ·ґУ¦ґпµЅ»ЇС§ЖЅєвЧґМ¬µДТАѕЭКЗ________ЎЈ
AЈ®ИЭЖчЦРС№ЗїІ»±д BЈ®»мєПЖшМеЦРc(CO)І»±д
CЈ®¦ФХэ(H2)ЈЅ¦ФДж(H2O) DЈ®c(CO2)ЈЅc(CO)
(4)ДіОВ¶ИПВЈ¬ЖЅєвЕЁ¶И·ыєППВКЅЈєc(CO2)Ў¤c(H2)ЈЅc(CO)Ў¤c(H2O)Ј¬КФЕР¶ПґЛК±µДОВ¶ИОЄ________ЎжЎЈ
(5)ФЪ800 ЎжК±Ј¬·ўЙъЙПКц·ґУ¦Ј¬ДіТ»К±їМІвµГИЭЖчДЪёчОпЦКµДЕЁ¶И·Ц±рОЄc(CO2)ОЄ2 molЎ¤LЈ1Ј¬c(H2)ОЄ1.5 molЎ¤LЈ1Ј¬c(CO)ОЄ1 molЎ¤LЈ1Ј¬c(H2O)ОЄ3 molЎ¤LЈ1Ј¬ФтПВТ»К±їМЈ¬·ґУ¦Пт________(МоЎ°ХэПтЎ±»тЎ°ДжПтЎ±)ЅшРРЎЈ