��Ŀ����
����Ŀ����һ��������ܱ������н������»�ѧ��Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��_________________________��
(2)�÷�ӦΪ____________(����ȡ����ȡ�)��Ӧ��
(3)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������________��
A��������ѹǿ���� B�����������c(CO)����
C������(H2)������(H2O) D��c(CO2)��c(CO)
(4)ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)��c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ________�档
(5)��800 ��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)Ϊ2 mol��L��1��c(H2)Ϊ1.5 mol��L��1��c(CO)Ϊ1 mol��L��1��c(H2O)Ϊ3 mol��L��1������һʱ�̣���Ӧ��________(���������)���С�
���𰸡�c(CO)c(H2O)/[c(CO2)c(H2)] ���� BC 830 ����
��������
����ƽ�ⳣ���ĺ����Ϸ���ʽ��д����ʽ�������¶ȶԻ�ѧƽ���Ӱ���ж�ƽ�ⳣ�����¶ȵĹ�ϵ�����ݻ�ѧƽ��ı��ʣ����淴Ӧ������ȣ��������������ʵ����ʵ�����Ũ�ȱ��ֲ��䣩�ж�ƽ���־��������ͬ�¶���Ũ������ƽ�ⳣ���Ĺ�ϵ�жϿ��淴Ӧ���еķ���
��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ����ӦCO2(g)��H2(g)![]() CO(g)��H2O(g)�Ļ�ѧƽ�ⳣ������ʽK��c(CO)��c(H2O)/[c(CO2)��c(H2)]��
CO(g)��H2O(g)�Ļ�ѧƽ�ⳣ������ʽK��c(CO)��c(H2O)/[c(CO2)��c(H2)]��
��2�����б������ݱ����������¶����ߣ��÷�Ӧƽ�ⳣ��K����ƽ���ƶ�ԭ��������ƽ�����ƣ�����Ӧ���ȡ�
��3��A�����з�Ӧ��������������䣬��PV��nRT�����º���ʱ������ѹǿ��Ȼ���䣬����������ѹǿ���䡱��һ���ǻ�ѧƽ��״̬��A��ѡ��
B���������������c(CO)���䡱ʱ���������ֳɷֵ�Ũ��Ҳ���䣬��Ϊ��ѧƽ��״̬��Bѡ��
C�������Ƿ�ƽ�⣬����(H2)������(H2O)��������(H2)������(H2O)��ʱ������(H2O)������(H2O)����Ϊ��ѧƽ��״̬��Cѡ��
D����c(CO2)��c(CO)����һ���ǻ�ѧƽ��״̬��D��ѡ��
�ʴ�ѡBC��
��4��ij�¶��£�ƽ��Ũ�ȷ���c(CO2)��c(H2)��c(CO)��c(H2O)����K��1�����ж�Ӧ�¶�Ϊ830�档
��5����800 ��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)Ϊ2 mol��L��1��c(H2)Ϊ1.5 mol��L��1��c(CO)Ϊ1 mol��L��1��c(H2O)Ϊ3 mol��L��1�����ʱ��Ũ����Qc����1mol/L��3mol/L��/��2mol/L��1.5mol/L����1��K��0.9�������һʱ�̣���Ӧ��������С�

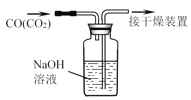
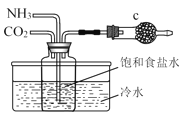
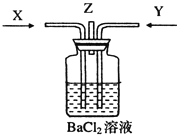
����Ŀ������ͼ��ʾװ�ü����Ӧ����ʱ�����ܴﵽĿ���ǣ� ��
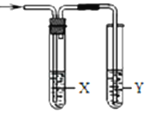
����װ�� ����װ��
���ɵ����� | �Լ� | �Լ� | |
| ��ʯ��ˮ��Ӧ��ȡ����Ȳ |
|
|
| ľ̿��Ũ | ���� | ����ʯ��ˮ |
|
| ˮ |
|
|
|
|
|
A. AB. BC. CD. D