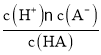��Ŀ����
����Ŀ����������������Һ�����ᡢNH3��H2O��NH4HSO4��NaOH��CH3COOH���ش��������⣺
��1����1LpH=2��HCl��Һ�ֱ���0.01mol��L-1��NH3�� H2O��Һx L��0.01 mol��L-1��NaOH��ҺyL��ַ�Ӧ�����ԣ�x��y��С��ϵΪ��y___x(����>����<������=��)��
��2��H+Ũ����ͬ�ĵ������������Һ�������CH3COOH���ֱ���п�۷�Ӧ����������һ����Һ�д���п�ۣ��ҷų�������������ͬ��������˵����ȷ����____(��д���)��
�ٷ�Ӧ����Ҫ��ʱ��CH3COOH >HCl
�ڿ�ʼ��Ӧʱ������HCl>CH3COOH
�۲μӷ�Ӧ��п�����ʵ���HCl=CH3COOH
�ܷ�Ӧ���̵�ƽ������CH3COOH>HCl
��HCl��Һ����п��ʣ��
��CH3COOH��Һ����п��ʣ��
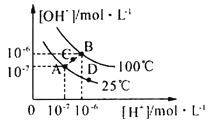
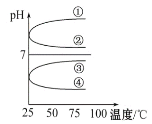
��3����������������ʵ���Ũ�ȵ�NH3��H2O��NH4HSO4��Һ��Ϻ������¶�(���ʲ���ֽ�)��ҺpH���¶ȱ仯��ͼ�е�____����(��д���)��
��4�������£���0.01mol��L-1NH4HSO4��Һ�еμ�0.01mol��L-1NaOH��Һ�����ԣ��õ�����Һ�У�c(Na+)+c(NH4+)___2c(SO42- )(����>����=������<��)����NH4HSO4������������Һ��ȡ���ᱵ������Һ��SO42-��ȫ��������Ӧ����Һ��pH___7(����>����=������<��)
��5��25��ʱ����amolNH4NO3����ˮ����Һ�����ԣ�ԭ����____(�����ӷ���ʽ��ʾ)�������Һ�μ�b L��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫___(��������������������������)�ƶ���
���𰸡�< �ۢܢ� �� = > NH4+��H2O![]() NH3��H2O��H+ ����
NH3��H2O��H+ ����
��������
(1)1LpH=2��HCl��Һ��0.01mol��L-1��NaOH��Һ1L��ַ�Ӧǡ�ó����ԣ�һԪǿ�ᡢһԪ������Һ�������ʵ�����Ϻ�ǡ������ǿ�������Σ���Һ�����ԣ���ʹ1LpH=2��HCl��Һ��0.01mol��L-1��NH3��H2O��Һ��ַ�Ӧ�����ԣ���ˮ���������1L������y<x��
(2)�������Ϸ������ٷ�Ӧ��ʼ����ϵ��룬������������Ũ�ȴ������ᣬ������Ũ��Խ��Ӧ����Ҫ��ʱ��Խ�̣�����CH3COOH��HCl���ʢٴ��ڿ�ʼ��Ӧʱ��Һ��������Ũ����ȣ����Է�Ӧʱ��������ȣ�HCl=CH3COOH���ʢڴ�����������������ȣ����Բμӷ�Ӧ��п�����ʵ�����HCl=CH3COOH���ʢ���ȷ���������ӵ�Ũ��Խ��Ӧ���̵�ƽ������Խ�죬���ڷ�Ӧ��Ӧ�����д�����������������ӣ����Դ�����������Ũ�ȴ������ᣬ��Ӧ����CH3COOH��HCl���ʢ���ȷ�������Ũ��С��CH3COOH��Ũ�ȣ��������ȣ�����������ʵ�������������ʵ����࣬��п�۷�Ӧ����������һ����Һ�д���п�ۣ��ҷų�����������ͬ��п�����ᷴӦ����㣬п����ᷴӦп���㣬�ʢ���ȷ������
(3)��������������ʵ���Ũ�ȵ�NH3��H2O��NH4HSO4��Һ��Ϻ�ǡ������(NH4)2SO4����Һ�����ԣ�pH<7�������¶ȴٽ�笠�����ˮ�⣬��Һ������ǿ��������ҺpH���¶ȱ仯��ͼ�еĢ����ߣ�
(4)���ݵ���غ㣬c(Na+)+c(NH4+)+c(H��)=2c(SO42-)��c(OH��)����Һ������c(OH��)= c(H��)������c(Na+)+c(NH4+)=2c(SO42-)��NH4HSO4������������Һ1:1��ϣ���Һ��SO42-ǡ����ȫ��������Ӧ���ӷ���ʽ��NH4����H����SO42-��Ba2+��2OH��![]() BaSO4��H2O��NH3��H2O����������NH3��H2O��������Һ�ʼ��ԣ�pH>7��
BaSO4��H2O��NH3��H2O����������NH3��H2O��������Һ�ʼ��ԣ�pH>7��
(5)NH4NO3��ǿ�������Σ�笠�����ˮ�⣬��Һ�����ԣ�ˮ�����ӷ���ʽ��NH4����H2O![]() NH3��H2O��H������ˮ����ˮ���룬���ԵμӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫�����ƶ���
NH3��H2O��H������ˮ����ˮ���룬���ԵμӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫�����ƶ���

����Ŀ����ϩ�����(CH2��CHCOOCH3)��һ����Ҫ���л�����ԭ�ϡ�ʵ�����Ʊ�������ϩ������ķ�ӦΪ��CH2��CHCOOH+CH3OH![]() CH2��CHCOOCH3+H2O���������£�
CH2��CHCOOCH3+H2O���������£�
����1����100mLԲ����ƿ�����μ���10.0g��ϩ�ᡢ�������Ƭ��10mL�״���2mLŨ���ᣬ���衣
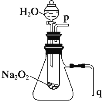
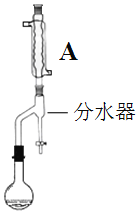
����2����ͼ������װ�ã�������ƿ�еĻ��Һ������ƿʢ��ͨ����ˮ���������ˮ����������ˮ���ɣ�ֹͣ���ȡ�
����3����ӦҺ��ȴ��������5%Na2CO3��Һ������ʳ��ˮ��ˮϴ�ӡ�������л��ࡣ
����4�����л����м���ˮNa2SO4���壬���˺������ռ�70��90����֡���ñ�ϩ�����������Ϊ6.45g��
�����õ�����Ϣ��
�ܶ� | �е� | �ܽ��� | ||
��ϩ�� | 1.05g��cm��3 | 141�� | ��ˮ���ܣ��������л��ܼ� | �ж� |
�״� | 0.79g��cm��3 | 65�� | ��ˮ���ܣ��������л��ܼ� | �ӷ����ж� |
��ϩ����� | 0.95g��cm��3 | 80.5�� | ������ˮ���������л��ܼ� | �ӷ� |
��ش��������⣺
��1������1�У��������Ƭ��Ŀ����________��
��2������2�У�ͼ����ʾװ��������A��������______��������Ϊ_______��
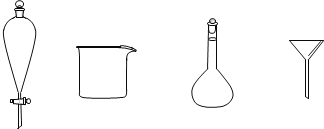
��3������3�У���5%Na2CO3��Һϴ�Ӻ����л���IJ�������Ϊ_______�������л���ʱ����Ҫ�õ����в��������е�_______(������)��
��4��ʵ���п������ɵ��л�������ṹ��ʽΪ_______ (��һ�ּ���)��
��5����ʵ���б�ϩ������IJ���Ϊ______%��