题目内容
7.已知具有碳碳双键结构的有机物可被碱性高锰酸钾溶液氧化成二元醇,如H2C═CH2$\stackrel{碱性KMnO_{4}}{→}$HOCH2CH2OH.现以CH2═C(CH3)2为原料按如图方式合成环状化合物D和高分子化合物G.
(1)写出F中官能团名称碳碳双键、酯基,A-→B的反应类型是氧化反应,C-→E的反应类型是消去反应,E-→F的反应类型是酯化反应(或取代反应).
(2)D的结构简式是
 ,G的结构简式是
,G的结构简式是 .
.(3)B-→C的化学方程式是
 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O.(4)E-→F的化学方程式是
 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.(5)C物质的同分异构体中,与C所含官能团种类和数目都相同的同分异构体有4种(不包括C).写出其中一种物质的结构简式HOCH2CH2CH2COOH(或CH3CHOHCH2COOH、HOCH2CH2CHOHCOOH、HOCH2CH(CH3)COOH).
分析 根据信息可知, 被碱性KMnO4溶液氧化生成A,则A为
被碱性KMnO4溶液氧化生成A,则A为 ;
; 被催化氧化生成B,则B为
被催化氧化生成B,则B为 ;
; 被催化氧化生成C,则C为
被催化氧化生成C,则C为 ;
; 发生消去反应生成E,则E为
发生消去反应生成E,则E为 ;
; 与CH3OH发生酯化反应生成F,则F为
与CH3OH发生酯化反应生成F,则F为 ;
; 发生加聚反应生成G,则G为
发生加聚反应生成G,则G为 ;比较C与D的分子式可知,两分子
;比较C与D的分子式可知,两分子 发生酯化反应生成环酯D,则D为
发生酯化反应生成环酯D,则D为 ,以此解答该题.
,以此解答该题.
解答 解:根据信息可知, 被碱性KMnO4溶液氧化生成A,则A为
被碱性KMnO4溶液氧化生成A,则A为 ;
; 被催化氧化生成B,则B为
被催化氧化生成B,则B为 ;
; 被催化氧化生成C,则C为
被催化氧化生成C,则C为 ;
; 发生消去反应生成E,则E为
发生消去反应生成E,则E为 ;
; 与CH3OH发生酯化反应生成F,则F为
与CH3OH发生酯化反应生成F,则F为 ;
; 发生加聚反应生成G,则G为
发生加聚反应生成G,则G为 ;比较C与D的分子式可知,两分子
;比较C与D的分子式可知,两分子 发生酯化反应生成环酯D,则D为
发生酯化反应生成环酯D,则D为 ,
,
(1)F的结构简式为 ,则F中官能团名称为:碳碳双键、酯基;
,则F中官能团名称为:碳碳双键、酯基;
A→B的反应为 被催化氧化生成
被催化氧化生成 ,该反应为氧化反应;
,该反应为氧化反应;
C→E的反应为 发生消去反应生成
发生消去反应生成 ;
;
E→F为 与CH3OH反应生成
与CH3OH反应生成 ,该反应为酯化反应,也属于取代反应,
,该反应为酯化反应,也属于取代反应,
故答案为:碳碳双键、酯基;氧化反应;消去反应;酯化反应(或取代反应);
(2)根据上面的分析可知,D的结构简式是 ,G的结构简式是
,G的结构简式是 ,
,
故答案为: ;
; ;
;
(3)B-→C的化学方程式是: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
故答案为: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O;
+Cu2O↓+2H2O;
(4)E→F的化学方程式为: +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为: +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O;
+H2O;
(5)C为 ,与C所含官能团种类和数目都相同的同分异构体为:HOCH2CH2CH2COOH、CH3CHOHCH2COOH、HOCH2CH2CHOHCOOH、HOCH2CH(CH3)COOH,共有4种,
,与C所含官能团种类和数目都相同的同分异构体为:HOCH2CH2CH2COOH、CH3CHOHCH2COOH、HOCH2CH2CHOHCOOH、HOCH2CH(CH3)COOH,共有4种,
故答案为:4;HOCH2CH2CH2COOH(或CH3CHOHCH2COOH、HOCH2CH2CHOHCOOH、HOCH2CH(CH3)COOH).
点评 本题考查有机物的推断,题目难度中等,明确有机物结构与性质为解答关键,注意把握题中信息反应原理,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及逻辑推理能力.

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案| A. | 一定有甲烷 | B. | 一定有甲烷和乙烯(C2H4) | ||
| C. | 可能有乙烷(C2H6) | D. | 一定有乙炔(C2H2) |
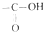 中的-OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )
中的-OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )| A. | CCl4 | B. | CH3COF | C. | CH3COCH2Cl | D. | CH2ClCOOH |
| A. | 无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,则原溶液一定含有CO32- | |
| B. | 无色溶液中加入 AgNO3溶液,有白色沉淀生成,则原溶液一定含有Cl- | |
| C. | 无色溶液中加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝,则原溶液中一定含有NH4+ | |
| D. | 无色溶液中加入BaCl2溶液有白色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液一定含有SO42- |
| A. | 1-丙醇与氧气的混合气体通过赤热的铜,生成丙醛 | |
| B. | 1-丙醇不能和氢卤酸发生反应 | |
| C. | 1-丙醇的沸点低于乙醇 | |
| D. | 1-丙醇、2-丙醇、丙醚互为同分异构体 |
| A. | 氢键比范德华力强,所以它属于化学键 | |
| B. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| C. | 由于NH3和H2O之间可形成分子间氢键,使氨在水中溶解度增大 | |
| D. | H2O是一种稳定的化合物,这是由于H2O之间形成氢键所致 |
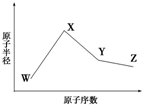 已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.
已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.
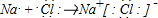
 石灰氰,是由氰氨化钙(CaCN2)、氧化钙和其他不溶性杂质构成的混合物.呈灰黑色,有特殊臭味.是一种碱性肥料,也是高效低毒多菌灵农药的主要原料之一,可用作除草剂、杀菌剂、杀虫剂等,可用于生产双氰胺、三聚氰胺和氰熔体等.
石灰氰,是由氰氨化钙(CaCN2)、氧化钙和其他不溶性杂质构成的混合物.呈灰黑色,有特殊臭味.是一种碱性肥料,也是高效低毒多菌灵农药的主要原料之一,可用作除草剂、杀菌剂、杀虫剂等,可用于生产双氰胺、三聚氰胺和氰熔体等. )俗称“蛋白精”,也可由氰氨化钙制得.在三聚氰胺分子中含有的σ键和π键数目之比为5:1.
)俗称“蛋白精”,也可由氰氨化钙制得.在三聚氰胺分子中含有的σ键和π键数目之比为5:1.