题目内容
【题目】(14分)硫酸铜晶体(CuSO4·5H2O)是铜盐中重要的无机化工原料,广泛应用于农业、电镀、饲料添加剂、催化剂、石油、选矿、油漆等行业。
Ⅰ.采用孔雀石[主要成分CuCO3·Cu(OH)2]、硫酸(70%)、氨水为原料制取硫酸铜晶体。其工艺流程如下:
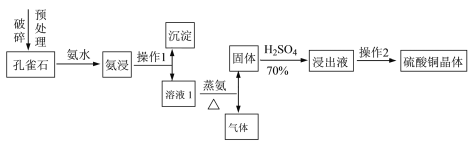
(1)预处理时要用破碎机将孔雀石破碎成粒子直径<1 mm,破碎的目的是____________________。
(2)已知氨浸时发生的反应为CuCO3·Cu(OH)2+8NH3·H2O![]() [Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:______________________。
[Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:______________________。
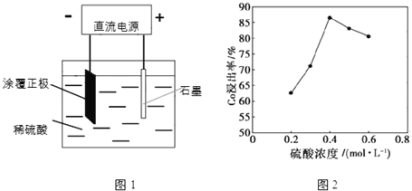
(3)蒸氨出来的气体有污染,需要净化处理,下图装置中合适的为___________(填标号);经吸收净化所得的溶液用途是_______________(任写一条)。

(4)操作2为一系列的操作,通过加热浓缩、冷却结晶、___________、洗涤、___________等操作得到硫酸铜晶体。
Ⅱ.采用金属铜单质制备硫酸铜晶体
(5)教材中用金属铜单质与浓硫酸反应制备硫酸铜,虽然生产工艺简洁,但在实际生产过程中不采用,其原因是______________________(任写两条)。
(6)某兴趣小组查阅资料得知:Cu+CuCl2![]() 2CuCl,4CuCl+O2+2H2O
2CuCl,4CuCl+O2+2H2O![]() 2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4
2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4![]() CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
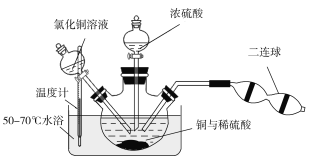
向铜和稀硫酸的混合物中加入氯化铜溶液,利用二连球鼓入空气,将铜溶解,当三颈烧瓶中呈乳状浑浊液时,滴加浓硫酸。
①盛装浓硫酸的仪器名称为___________。
②装置中加入CuCl2的作用是______________;最后可以利用重结晶的方法纯化硫酸铜晶体的原因为______________________。
③若开始时加入a g铜粉,含b g氯化铜溶质的氯化铜溶液,最后制得c g CuSO4·5H2O,假设整个过程中杂质不参与反应且不结晶,每步反应都进行得比较完全,则原铜粉的纯度为________。
【答案】增大反应物接触面积,提高氨浸的效率 [Cu(NH3)4]2(OH)2CO3![]() 2CuO+CO2↑+8NH3↑+H2O A 制化学肥料等 过滤 干燥 产生有毒的气体,污染环境;原材料利用率低;浓硫酸有强腐蚀性 分液漏斗 做催化剂 氯化铜的溶解度在常温下比硫酸铜晶体大得多,且氯化铜的溶解度随温度的变化程度不大(合理即可)
2CuO+CO2↑+8NH3↑+H2O A 制化学肥料等 过滤 干燥 产生有毒的气体,污染环境;原材料利用率低;浓硫酸有强腐蚀性 分液漏斗 做催化剂 氯化铜的溶解度在常温下比硫酸铜晶体大得多,且氯化铜的溶解度随温度的变化程度不大(合理即可) ![]() ×100%(或
×100%(或![]() %)
%)
【解析】
(1)破碎机把孔雀石破碎成细小颗粒,增大了与氨水接触面积,使铜与氨充分络合,提高氨浸的效率及浸取率。
(2)由题意可知,氨浸时生成[Cu(NH3)4]2(OH)2CO3,加热蒸氨的意思为加热时[Cu(NH3)4]2(OH)2CO3分解生成氨气,由[Cu(NH3)4]2(OH)2CO3的组成可知还会生成CO2、氧化铜和水,其反应方程式为[Cu(NH3)4]2(OH)2CO3![]() 2CuO+CO2↑+8NH3↑+H2O。
2CuO+CO2↑+8NH3↑+H2O。
(3)蒸氨出来的气体有氨气和二氧化碳,氨气有污染,需要通入硫酸净化处理生成硫酸铵,为了防止倒吸,合适的装置为A;净化后生成硫酸铵溶液,其用途是可以制备化学肥料等。
(4)由题意可知,操作2为硫酸铜溶液变成硫酸铜晶体,操作为加热浓缩、冷却结晶、过滤、洗涤、干燥。
(5)课本中直接利用铜与浓硫酸反应会产生有毒的气体二氧化硫;这样既污染环境又使原材料利用率低;而且浓硫酸有强腐蚀性,直接使用危险性较大。
(6)①盛装浓硫酸的仪器为分液漏斗。
②由题意可知,氯化铜虽然参与反应,但最后又生成了等量的氯化铜,根据催化剂的定义可知氯化铜在此反应过程中做催化剂。因为氯化铜的溶解度在常温下比硫酸铜晶体大得多,在重结晶纯化硫酸铜晶体时可以使二者分离,同时氯化铜的溶解度随温度的变化程度不大,可使氯化铜保持在母液中,在下一次制备硫酸铜晶体时继续做催化剂使用。
③由题意可知铜粉全部生成硫酸铜晶体(因氯化铜为催化剂,氯化铜中的铜最终不会生成硫酸铜晶体),硫酸铜晶体中的铜元素质量为![]() g,则铜粉的纯度为
g,则铜粉的纯度为![]() ×100%或化简为
×100%或化简为![]() %。
%。

【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
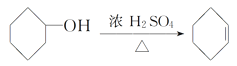 +H2O
+H2O

可能用到的有关数据如下:
相对分子质量 | 密度/ g·cm-3 | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置b的名称是______。
(2)加入碎瓷片的作用是________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填字母,下同)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为________________。
(4)分液漏斗在使用前须清洗干净并______;在本实验分离过程中,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是______________。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________。
A 圆底烧瓶 B 温度计 C 吸滤瓶 D 球形冷凝管 E 接收器
(7)本实验所得到的环己烯产率是________。
A.41% B.50% C.61% D.70%