题目内容
【题目】某化工厂生产的某产品A只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等). 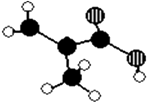
(1)该产品的结构简式为 , 含有的官能团名称 ,
(2)该化合物的核磁共振氢谱中有个吸收峰.
(3)(填序号)下列物质中,与A互为同分异构体的是 , 与A互为同系物的是 ①CH3CH=CHCOOH ②CH2=CHCOOCH3
③CH3CH2CH=CHCOOH ④CH3CH(CH3)COOH
(4)写出该物质与甲醇反应的化学方程式: .
【答案】
(1)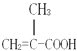 ;碳碳双键;羧基
;碳碳双键;羧基
(2)3
(3)①②;③
(4)
【解析】解:(1)该物质的结构简式为 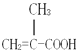 ;含有官能团是碳碳双键和羧基,所以答案是:
;含有官能团是碳碳双键和羧基,所以答案是: 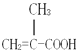 ;碳碳双键和羧基;(2)有几种氢原子其核磁共振氢谱中就有几个吸收峰,该分子中含有3种氢原子,所以有3个吸收峰,所以答案是:3;(3)分子式相同、结构不同的有机物互称同分异构体;结构相似、在分子组成上相差一个或n个﹣CH2原子团的有机物互称同系物,所以互为同分异构体的是①②,互为同系物的是③,所以答案是:①②;③;(4)在浓硫酸作催化剂、加热条件下,该物质和甲醇发生酯化反应,反应方程式为
;碳碳双键和羧基;(2)有几种氢原子其核磁共振氢谱中就有几个吸收峰,该分子中含有3种氢原子,所以有3个吸收峰,所以答案是:3;(3)分子式相同、结构不同的有机物互称同分异构体;结构相似、在分子组成上相差一个或n个﹣CH2原子团的有机物互称同系物,所以互为同分异构体的是①②,互为同系物的是③,所以答案是:①②;③;(4)在浓硫酸作催化剂、加热条件下,该物质和甲醇发生酯化反应,反应方程式为  ,
,
所以答案是:  .
.
【考点精析】利用有机物的结构和性质对题目进行判断即可得到答案,需要熟知有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】某学习小组用如下装置(支撑仪器略去)探究乙醇的催化氧化反应和乙醛的性质. 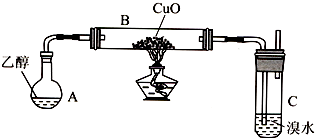
(1)实验开始时,对A进行水浴加热,其目的是 .
(2)B中反应方程式为 .
(3)若装置C中开始发生倒吸,则采取的应急措施是(填编号).
A.移去图中的酒精灯
B.将C中橡皮塞上的短导气管拔出
C.将B尾端的乳胶管取下
D.将A与B之间的乳胶管取下
(4)探究:充分反应后,观察到溴水完全褪色.学习小组通过测定反应前溴水中n(Br2)与反应后溶液中n(Br﹣)来确定乙醛使溴水褪色的原因. ①假设.请写出假设1的反应类型.
假设1:CH3CHO+Br2→CH2BrCHO+HBr;反应
假设2:CH3CHO+Br2→CH3CHBrOBr; 加成反应
假设3:CH3CHO+Br2+H2O→CH3COOH+2HBr. 氧化反应
②结论:若实验测得n(Br2)=0.005mol,n(Br﹣)=0.01mol,则证明假设正确.
(5)欲检验乙醇中混有的少量乙醛,甲乙丙三同学设计实验如表:
试剂、用品 | 预期现象 | |
甲 | 酸性高锰酸钾溶液 | 溶液紫红色褪去 |
乙 | 溴水 | 溴水褪色 |
丙 | 铜丝 酒精灯 | 铜丝由黑色变成光亮的红色 |
则上述方案中你认为能正确完成乙醛的检验的是(填甲、乙、丙)