题目内容
将一小块钠投入MgCl2溶液中,下列对有关实验结果的预测正确的是
| A.钠溶解,底部有银白色金属析出,并且有气体产生 |
| B.只有气体产生 |
| C.只有沉淀产生 |
| D.既有沉淀产生,又有气体产生 |
D
解析试题分析:钠的密度小于水的密度,且熔点较低,钠的性质很活泼,能和水反应生成氢气和氢氧化钠。由于受力不均导致四处游动,氢氧化钠和氯化镁溶液反应生成氢氧化镁白色沉淀,溶剂的质量减少,导致溶液变成过饱和溶液,会析出溶质氯化镁。所以将金属钠投入饱和MgCl2溶液中现象为,开始时钠浮在液面上、四处游动并熔成小球,有白色沉淀生成,会析出部分溶质,故正确的答案选D。
考点:考查

练习册系列答案
相关题目
我省庐江县有丰富的钒矿资源——明矾,其主成分为KAl(SO4)2·12H2O。下列有关说法正确的是
| A.明矾既可以除去水中的悬浮物,也可以杀菌消毒 |
| B.可以通过电解明矾溶液来制取Al |
| C.用酒精灯加热铝箔至熔化,铝并不滴落,说明氧化铝的熔点比铝高 |
| D.可以用在某溶液中加入盐酸酸化的氯化钡溶液的方法来确定该溶液中是否含有SO42- |
下列物质中,既能与盐酸反应又能与NaOH溶液反应的是( )
①NaHCO3 ②Al(OH)3 ③ Al2O3 ④ (NH4)2SO3 ⑤Al
| A.①② | B.②③⑤ | C.①②④⑤ | D.全部 |
为使以面粉为原料的面包松软可口,通常用碳酸氢钠作发泡剂,因为它
①热稳定性差②增加甜味③产生二氧化碳④提供钠离子。其中合理的是
| A.②③ | B.①③ | C.①④ | D.③④ |
测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案不合理的是( )
| A.取a克混合物充分加热,减重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
通过对金属钠与水反应现象的观察,不能分析得出的结论是( )
| A.金属钠熔点低 | B.金属钠导电性强 |
| C.金属钠密度小 | D.金属钠化学性质活泼[来源 |
将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A.铁恰好将Fe3+全部还原 |
| B.往反应后溶液中滴入KSCN溶液,不显红色 |
| C.溶液变为浅绿色 |
| D.Fe2+和Fe3+物质的量之比为6:1 |
一定量碳酸氢钠与过氧化钠的混合物在密闭体系中充分加热后,排出气体,固体残留物组成不可能是( )
| A.NaOH和Na2CO3 | B.Na2O2、NaOH和Na2CO3 |
| C.NaOH | D.Na2CO3 |
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是( )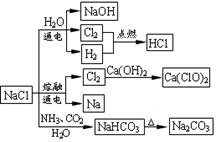
| A.石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| B.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C.常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| D.图中所示转化反应都是氧化还原反应 |