题目内容
向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应: 。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
 。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )| A.0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 |
| B.1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 |
| C.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 |
| D.0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
B
A 一边倒之后,1.5 mol CO+3mol H2O(g) 体积比是1:2,相当于在原平衡的条件下,增大压强,平衡不移动,CO的体积分数仍为为x
B 一边倒后,2 mol CO+2 mol H2O(g),体积比大于1:2,相当于增大了CO浓度,CO的体积分数大于x,选B
C 一边倒后,0.9 mol CO+1.9 mol H2O(g) 体积比小于1:2,相当于增大了 H2O(g)的浓度,平衡右移,CO浓度减小,CO的体积分数小于x
D 一边倒后,1 mol CO+2 mol H2O(g),和原平衡一样,CO的体积分数为x。
B 一边倒后,2 mol CO+2 mol H2O(g),体积比大于1:2,相当于增大了CO浓度,CO的体积分数大于x,选B
C 一边倒后,0.9 mol CO+1.9 mol H2O(g) 体积比小于1:2,相当于增大了 H2O(g)的浓度,平衡右移,CO浓度减小,CO的体积分数小于x
D 一边倒后,1 mol CO+2 mol H2O(g),和原平衡一样,CO的体积分数为x。

练习册系列答案
 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
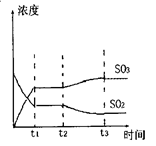
 2SO3(g) △H=-196kJ/mol。
2SO3(g) △H=-196kJ/mol。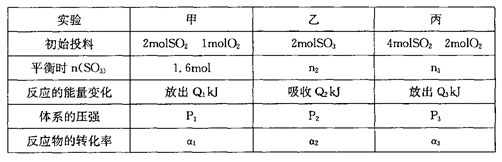
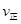 _______
_______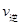
 CO2(g)+H2(g),达到平衡时测得CO2为0.6mol。再通入4mol H2O(g),达到新平衡后,CO2的物质的量为
CO2(g)+H2(g),达到平衡时测得CO2为0.6mol。再通入4mol H2O(g),达到新平衡后,CO2的物质的量为  C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1,c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。下列说法正确的是 ( )
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1,c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。下列说法正确的是 ( )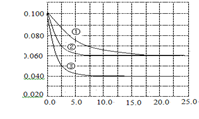
 y C(g),如图表示在不同条件下反应物B的体积分数φ(B)随时间变化的关系,据此判断
y C(g),如图表示在不同条件下反应物B的体积分数φ(B)随时间变化的关系,据此判断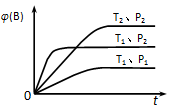
 H+(aq) + In-(aq)
H+(aq) + In-(aq) zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,测
zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,测 CH3OCH3(g)+CO2(g) △H< 0。一定条件下得密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
CH3OCH3(g)+CO2(g) △H< 0。一定条件下得密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。 CO(g)+H2(g);②CO(g)+H2O(g)
CO(g)+H2(g);②CO(g)+H2O(g)