题目内容
【题目】氧化亚铜(Cu2O)是船舶防污剂的首选,可利用印刷电路板酸性蚀刻液(CuCl42-、Cl-、H+)和碱性蚀刻液[Cu(NH3)42+、NH4+、NH3、Cl-]来制备,工艺流程如下:
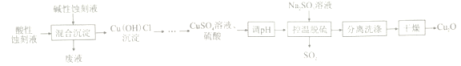
已知:强酸条件下,2Cu+==Cu+Cu2+
(1)不同pH下“混合沉淀”实验结果见下表。由表可知,pH应控制在______左右。
pH | 4.00 | 4.50 | 5.40 | 6.20 | 6.50 | 7.00 | 8.00 | 8.50 |
废液含铜量/g.L-1 | 19.5 | 2.4 | 2.0 | 0.3 | 0.2 | 2.0 | 8.3 | 17.0 |
(2)“混合沉淀”中废液的主要成分为______________(填化学式)
(3)“控温脱硫”生成Cu2O的离子方程式为_________;该过程产生的SO2经_____(填化学式)处理后生成可循环物质Na2SO3。
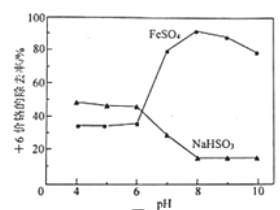
(4)“控温脱硫”过程中温度对Cu2O的产率影响及SO2在水中溶解度随温度变化如图所示:
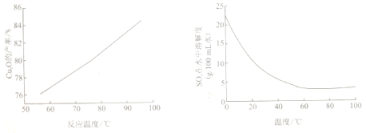
下列说法正确的是_____
a.在60℃以下,温度越高,SO2越易逸出,有利于提高生产中硫原子利用率
b.反应温度的变化是影响Cu2O产率的主要因素
c.结合工业生产实际,温度应控制在溶液呈沸腾状态
d.低温时,Cu2O产率较低与SO2低温时的溶解度较大有关
(5)检验Cu2O是否洗涤干净的方法是______________________________。
(6)某工厂用V1,L含铜量120g·L-1的酸性蚀刻液和V2L含铜量160g·L-1的碱性蚀刻液制备Cu2O,最终得到产品mg,产率为____%。
【答案】 6.50 NH4Cl 2Cu2+ + 3SO32- = Cu2O↓ + SO42- + 2SO2↑ NaOH(写成 Na2CO3 或 NaHCO3 均给分 ) acd 取最后一次洗涤液少许,加入 BaCl2 溶液,若无白色沉淀生成,则已经洗净 20m/(27V1 + 36V2)
【解析】本题考查的是物质的制备实验方案的设计,难度较大。
(1)根据表中数据分析pH在6.50左右废液中含铜量最少。(2)从酸性蚀刻液和碱性蚀刻液的成分分析,二者混合后废液的主要成分为氯化铵;(3)铜离子和亚硫酸根离子反应生成氧化亚铜和硫酸根离子和二氧化硫,离子方程式为:2Cu2+ + 3SO32- = Cu2O↓ + SO42- + 2SO2↑;二氧化硫与 NaOH或 Na2CO3 或 NaHCO3 都可以生成亚硫酸钠。 (4) a.在60℃以下,温度越高,SO2越易逸出,反应不断正向进行,有利于提高生产中硫原子利用率,故正确;b.从图分析,在60度以后温度对二氧化硫的影响不大,因此反应温度的变化不是影响Cu2O产率的主要因素,故错误;c.结合工业生产实际,温度高有利于生成氧化亚铜,因此温度控制在溶液呈沸腾状态有利于脱硫,故正确;d.低温时,二氧化硫不能及时逸出,使氧化亚铜的产率降低,因此Cu2O产率较低与SO2低温时的溶解度较大有关,故正确,故答案为:acd; (5). 反应过程中生成硫酸根离子,所以检验洗涤液是否含有硫酸根离子即可,实验方法为取最后一次洗涤液少许,加入 BaCl2 溶液,若无白色沉淀生成,则已经洗净; (6) 用V1,L含铜量120g·L-1的酸性蚀刻液和V2L含铜量160g·L-1的碱性蚀刻液含铜的质量为(V1 ×120+V2×160)g,则生成的氧化亚铜的质量为![]() ,产率为
,产率为![]() ×100%= 20m/(27V1 + 36V2)%。
×100%= 20m/(27V1 + 36V2)%。

【题目】氮及其化合物在工农业生产生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
(1)已知:N2(g)+O2(g)==2NO(g) △H =+180.5kJ·mol-1
C(s)+O2(g)=CO2(g) △H =-393.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H =-221kJ·mol-1
若某反应的平衡常数表达式为:k=[c(N2)·c2(CO2)]/[c2(NO)·c(CO)],请写出此反应的热化学方程式_______。
(2)N2O5在一定条件下可发生分解:2N2O5(g)![]() 4NO2(g)+O2(g),某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
4NO2(g)+O2(g),某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
C(N2O6)/(mol/L) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①反应开始时体系压强为P0,第3.00 min时体系压强为P1,则P1:P0=_______;2min~5.00min 内,O2 的 平 均反应速率为_____________。
②一定温度下,在恒容密闭容器中充人一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___。
a.NO2 和O2 的浓度比保持不变 b.容器中压强不再变化
c.2v正(NO2)= v逆(N2 O5 ) d.气体的平均相对分子质量为43.2,且保持不变
(3)将2molN2 和4mo1H2 置于lL的恒容密闭容器中反应。测得不同温度、不同时间段内合成NH3 反应中N2 的转化率,得到数据如下表:

表中a、b、25%三者由大到小的顺序为_____,理由是_____。
(4)将(3)中实验得到的混合气体通入醋酸溶液中并恢复到25℃,当两者恰好反应时,生成的CH3COONH4溶液呈中性,则25℃时NH3·H2O的电离平衡常数Kb=______(已知:25℃时0.18mol/LCH3COOH 溶液中c(H+)=1.8×10-3mol/L)。