题目内容
【题目】下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题:
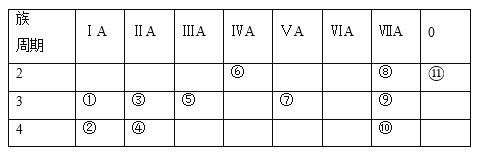
(1)这11种元素中,化学性质最不活泼的元素是______(填元素符号,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的化学方程式__________。
(2)元素④的离子结构示意图为___________。
【答案】Ne F 2K+2H2O═2KOH+H2↑ 
【解析】
根据元素在周期表中位置分析元素的种类,根据核外电子排布特征分析元素的性质,根据元素性质分析书写相关反应方程式;根据核外电子排布情况画出离子结构示意图。
根据元素在周期表中的位置可知,①②③④⑤⑥⑦⑧⑨⑩分别为Na、K、Mg、Ca、Al、C.P、F.Cl、Br、Ne元素,
(1)这11种元素中,化学性质最不活泼的元素是稀有气体Ne;F非金属性最强,其得电子能力最强;所列元素中金属性最强的为K,则失电子能力最强的单质为金属K,K与水反应生成KOH和氢气,该反应的化学方程式是:2K+2H2O═2KOH+H2↑,故答案为:Ne;F;2K+2H2O═2KOH+H2↑;
(2)元素④的离子为钙离子,钙离子结构示意图为 ,故答案为:
,故答案为: 。
。

练习册系列答案
相关题目
【题目】下列实验结果不能作为相应定律或原理的证据之一的是( )
A | B | C | D | |
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 | |
实验方案 |
|
|
|
|
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡 试管中出现浑浊 | 测得 |
|
(B中试剂为浓盐酸、碳酸钠溶液、硅酸钠溶液)
A.AB.BC.CD.D