题目内容
10.在50mL试管中充满15mL Cl2和35mL H2,受强光照射一定时间后,试管倒立在冷水中,进入试管中的水的体积是( )| A. | 30mL | B. | 25mL | C. | 20mL | D. | 0mL |
分析 发生反应:Cl2+H2=2HCl,反应后气体总体积不变,剩余氢气为35mL-15mL=20mL,生成HCl为30mL,进入试管中水的体积等于HCl的体积.
解答 解:由Cl2+H2=2HCl,可知15mL氯气完全反应消耗氢气为15mL,故氢气剩余,剩余氢气为35mL-15mL=20mL,可知反应后气体总体积不变,生成HCl为15mL×2=30mL,进入试管中水的体积等于HCl的体积,即进入试管中的水的体积是30mL,
故选:A.
点评 本题考查化学方程式有关计算,涉及过量计算,难度不大,侧重对基础知识的巩固.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
1.下列离子方程式书写正确的是( )
| A. | Ca(HCO3)2溶液中滴入过量NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向NaAlO2溶液中通入过量的CO2:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 0.01 mol•L-1 的NH4Al(SO4)2溶液与0.02 mol•L-1的Ba(OH)2溶液等体积混合:Al3++2SO42-+NH4++2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 向Ca(ClO)2溶液中通入过量的SO2:ClO-+SO2+H2O═HClO+HSO3- |
18.下列有关元素周期律的叙述正确的是( )
| A. | 随着原子序数的递增,原子最外层电子数总是从1到8重复出现 | |
| B. | 元素的性质随着原子序数的递增而呈周期性变化 | |
| C. | 随着原子序数的递增,仅有元素的化合价出现周期性的变化 | |
| D. | 元素性质的周期性变化是仅指原子半径的周期性变化 |
15.下列各组物质中互为同系物的是 ( )
| A. | 甲醇、乙二醇 | B. | 丙三醇、乙二醇 | C. | 甲醚、乙醇 | D. | 甲醇、2-丙醇 |
2.下列说法中不正确的是( )
| A. | Si是一种非金属主族元素,其晶体可用于制作计算机芯片 | |
| B. | 光导纤维和石英玻璃主要成分都是二氧化硅 | |
| C. | 过量CO2通入Na2SiO3溶液,最终无沉淀产生 | |
| D. | 硅胶疏松多孔,可用作催化剂的载体 |
20.下列物质中,所含分子个数最多的是( )
| A. | 0.05mol H3PO4 | B. | 1.204×1024个CH4 | C. | 2.0 mol HCl | D. | 3.5mol N2 |
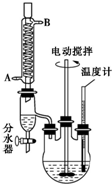 DIDP常温下为液体,工业上常用作树脂或塑料增塑剂,密度约为0.966g•cm-3,不溶于水,易溶于有机溶剂,制备邻苯二甲酸二异癸酯(DIDP)的主要操作步骤如下(夹持和加热装置已略去):
DIDP常温下为液体,工业上常用作树脂或塑料增塑剂,密度约为0.966g•cm-3,不溶于水,易溶于有机溶剂,制备邻苯二甲酸二异癸酯(DIDP)的主要操作步骤如下(夹持和加热装置已略去):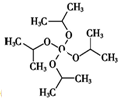 )、95.7g异癸醇及邻苯二甲酸酐;
)、95.7g异癸醇及邻苯二甲酸酐;