题目内容
20.写出下列反应的化学方程式或离子方程式.(1)1g乙醇C2H5OH完全燃烧放出热量12kJ,写出表示乙醇标准燃烧热的热化学方程式:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-552 kJ•mol-1
(2)用惰性电极电解CuSO4溶液的化学方程式:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4.
分析 (1)依据1g乙醇完全燃烧生成CO2和液态水时放热12kJ,结合燃烧热的定义计算求出1mol乙醇完全燃烧放出的热量,然后写出热化学方程式;
解答 解:(1)1g乙醇完全燃烧生成CO2和液态水时放热12kJ,则1mol乙醇,质量为46g,完全燃烧生成稳定的氧化物放出的热量为:46×12kJ=552KJ,其燃烧热的热化学方程式为:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-552 kJ•mol-1,
故答案为:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-552 kJ•mol-1;
(2)用惰性电极电解硫酸铜溶液时,阳极上氢氧根离子放电生成氧气、阴极上铜离子放电生成Cu,化学方程式为2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4
故答案为:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4.
点评 本题考查了方程式的书写,明确反应的实质是解题关键,题目难度不大.

练习册系列答案
相关题目
11.下列叙述错误的是( )
| A. | 用新制的银氨溶液可区分甲酸甲酯和乙醛 | |
| B. | 用溴水一种试剂可鉴别甲苯、乙烯、乙醇、四氯化碳四种液体 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用金属钠可区分乙醇和乙醚 |
5.下列过程应用于工业生产的是( )
| A. | 锌与稀硫酸反应制取氢气 | B. | 氯化铵和氢氧化钙制取氨气 | ||
| C. | 浓盐酸和二氧化锰反应制取氯气 | D. | 氯气与石灰乳反应制取漂白粉 |
12.今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-,现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.792L(已换算成标准状况,且设气体全部逸出);②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.根据上述实验,以下推测正确的是( )
| A. | 一定不存在Ba2+,NH4+可能存在 | B. | CO32- 一定存在 | ||
| C. | Na+一定存在 | D. | 一定不存在Cl- |
9.某有机物A的结构为( ),下列关于A的叙述中错误的是( )
),下列关于A的叙述中错误的是( )
 ),下列关于A的叙述中错误的是( )
),下列关于A的叙述中错误的是( )| A. | 该物质在一定条件下能发生缩聚反应 | |
| B. | 该物质的核磁共振氢谱(1H-NMR)上共有7个峰 | |
| C. | 1 mol该物质最多能与含1 mol Br2的溴水发生取代反应 | |
| D. | 该物质能与Na、NaOH、NaHCO3、盐酸等物质反应 |
10.在50mL试管中充满15mL Cl2和35mL H2,受强光照射一定时间后,试管倒立在冷水中,进入试管中的水的体积是( )
| A. | 30mL | B. | 25mL | C. | 20mL | D. | 0mL |
 :
:
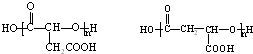 .
. .
. .
.