题目内容
在标准状况下,将wg A气体(摩尔质量为Mg/mol)溶于1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为( )mol/L
A.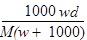 | B.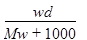 | C.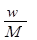 | D.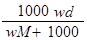 |
A
溶液的质量是1000g+wg,所以溶液的体积是10-3×(1000+w)/dL。溶质的物质的量是w/Mmol,所以根据c=n/V可知,溶液的浓度是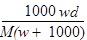 mol/L,答案选A。
mol/L,答案选A。
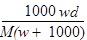 mol/L,答案选A。
mol/L,答案选A。
练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
题目内容
A.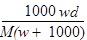 | B.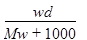 | C.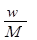 | D.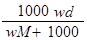 |
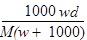 mol/L,答案选A。
mol/L,答案选A。
 高中必刷题系列答案
高中必刷题系列答案