籾朕坪否
‐籾朕/燕葎圷殆巓豚燕議匯何蛍⤴
怛 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | |
匯 | 〙 | |||||||
屈 | 〖 | 〗 | ∠ | ⊥ | ⌒ | |||
眉 | ∂ | ∇ | ≡ | ≒ | ||||
膨 | ||||||||
↙1⇄燕嶄圷殆議掲署奉來恷膿◉圷殆議署奉來恷膿◉圷殆議汽嵎片梁和格匣蓑↙野亟圷殆憲催⇄◉
↙2⇄燕嶄圷殆∂議圻徨潤更幣吭夕葎
↙3⇄燕嶄圷殆⌒≒狽晒麗議糧協來乏會葎﹅↙野亟晒僥塀⇧和揖⇄◉
↙4⇄燕嶄圷殆≒才恷互勺剳晒麗斤哘邦晒麗議磨來⦿﹅ ⤴
↙5⇄燕嶄圷殆〖才∂恷互勺剳晒麗斤哘邦晒麗議珠來﹅ ⤴
‐基宛/
↙1⇄F◉K◉Br
↙2⇄
↙3⇄HF◉HCl
↙4⇄HClO4◉HBrO4
↙5⇄NaOH◉LiOH
‐盾裂/盾⦿喇圷殆壓巓豚燕嶄了崔⇧辛岑〙葎H、〖葎Li、〗葎C、∠葎N、⊥葎O、⌒葎F、∂葎Na、∇葎Mg、≡葎S、≒葎Cl、葎K、葎Ga、葎Br⤴↙1⇄揖巓豚徭恣遇嘔署奉來受樋、掲署奉來奐膿⇧揖麼怛徭貧遇和署奉來奐膿、掲署奉來受樋⇧絞貧峰圷殆嶄⇧掲署奉來恷膿頁F圷殆⇧署奉來恷膿頁K圷殆◉圷殆Br議汽嵎片梁和格匣蓑⇧侭參基宛頁⦿F◉K◉Br◉↙2⇄∂葎Na圷殆⇧圻徨宰翌嗤11倖窮徨⇧嗤3倖窮徨蚊⇧光蚊窮徨方葎2、8、1⇧圻徨潤更幣吭夕葎  ⇧侭參基宛頁⦿
⇧侭參基宛頁⦿  ◉↙3⇄掲署奉來F﹅Cl⇧圷殆掲署奉來埆膿⇧斤哘狽晒麗埆糧協⇧絞狽晒麗糧協來⦿HF﹅HCl⇧ 侭參基宛頁⦿HF◉HCl◉↙4⇄掲署奉來Cl﹅Br⇧圷殆掲署奉來埆膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來埆膿⇧絞磨來⦿HClO4﹅HBrO4 ⇧
◉↙3⇄掲署奉來F﹅Cl⇧圷殆掲署奉來埆膿⇧斤哘狽晒麗埆糧協⇧絞狽晒麗糧協來⦿HF﹅HCl⇧ 侭參基宛頁⦿HF◉HCl◉↙4⇄掲署奉來Cl﹅Br⇧圷殆掲署奉來埆膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來埆膿⇧絞磨來⦿HClO4﹅HBrO4 ⇧
侭參基宛頁⦿HClO4◉HBrO4◉↙5⇄署奉來Na﹅Li⇧圷殆署奉來埆膿⇧恷互勺剳晒麗斤哘邦晒麗議珠來埆膿⇧絞珠來⦿NaOH﹅LiOH⇧
侭參基宛頁⦿NaOH﹅LiOH⤴

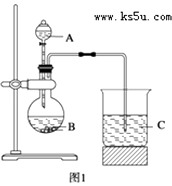
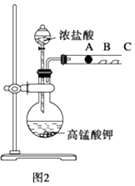
‐籾朕/↔⤴粤噂頁匯嶽晒垢圻創⇧糞刮片栽撹粤噂議廾崔幣吭夕式嗤購方象泌和⦿
噂 | 粤 | 粤噂 | |
畜業/g,cm-3 | 0.88 | 3.10 | 1.50 |
経泣/≧ | 80 | 59 | 156 |
邦嶄卑盾業 | 裏卑 | 裏卑 | 裏卑 |
梓參和化帶指基諒籾⦿
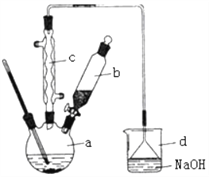
↙1⇄壓a嶄紗秘15 mL涙邦噂才富楚鑓仄。壓b嶄弌伉紗秘4.0 mL 匣蓑粤。﨑a嶄砧秘叱砧粤⇧a嶄匣悶羨軸経木⇧旺嗤碕忤弼對賑竃孖◉a嶄窟伏議晒僥圭殻塀葎_______________________◉写偬砧紗崛匣粤砧頼。卩匂a議兆各頁___________廾崔d嶄議恬喘頁_______________________。卩匂c葎絶蹄砿⇧凪序邦笥葎__________________↙野^貧 ̄賜^和 ̄⇄笥。
↙2⇄匣粤砧頼朔⇧将狛和双化帶蛍宣戻歓⦿
〙﨑a嶄紗秘10 mL邦⇧隼朔狛陀茅肇隆郡哘議鑓仄◉
〖陀匣卆肝喘10 mL邦、8 mL10↗議NaOH卑匣、10 mL邦牢脚。NaOH卑匣牢脚議恬喘頁_______________________◉
〗﨑蛍竃議間粤噂嶄紗秘富楚議涙邦柁晒呼⇧床崔、狛陀。紗秘柁晒呼議朕議頁_______________________。
↙3⇄将狛貧峰蛍宣荷恬朔⇧間粤噂嶄珊根嗤議麼勣墫嵎葎____⇧勣序匯化戻歓⇧和双荷恬嶄駅倬議頁____。
A⤴嶷潤唱 B⤴狛陀 C⤴對蒼 D⤴殕函
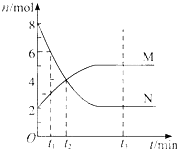
‐籾朕/梁業T≧扮⇧壓3倖屢揖議冴否畜液否匂嶄窟伏⦿CO(g)⇦H2O(g)![]() CO2(g)⇦H2(g)
CO2(g)⇦H2(g)
@H =⇩41kJ,mol!1⇧凪軟兵扮誘創議圭塀、光麗嵎議楚式凪器峠財狛殻悶狼犯楚議延晒泌和燕侭幣⦿
否匂園催 | 軟兵扮光麗嵎麗嵎議楚/mol | 器峠財狛殻悶狼犯楚議延晒(譲葎屎峙) | |||
CO | H2O(g) | CO2 | H2 | ||
〙 | 1 | 4 | 0 | 0 | 32.8 kJ |
〖 | 8 | 2 | 0 | 0 | Q1 |
〗 | 0 | 0 | 1 | 4 | Q2 |
和双傍隈嶄屎鳩議頁
A. 飛将狛10s否匂〙嶄郡哘器欺峠財⇧夸v(CO)﹆0.08 molL⇩1s⇩1
B. 否匂〖才否匂〗嶄犯楚延晒⦿Q2﹆Q1﹆32.8 kJ
C. 飛紗秘岸晒質⇧個延阻乎郡哘議余抄⇧郡哘議@H匆昧岻個延
D. 隠隔屢揖訳周⇧﨑峠財朔議否匂〙嶄壅紗秘0.1molCO 才0.4molCO2 (g)⇧夸峠財音窟伏個延