题目内容
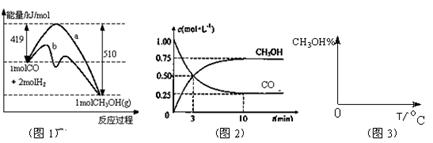
(10分)工业上用CO生产燃料甲醇。一定条件下发生反应: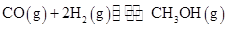 。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
请回答下列问题:
(1)在“图1”中,曲线 (填a或b)表示使用了催化剂;该反应属于 (填吸热、放热)反应。
(2)下列说法正确的是
(3)从反应开始到建立平衡,v(H2)= ;该温度下CO(g)+2H2(g)  CH3OH(g)的化学平衡常数为 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数 (填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数 (填“增大”、“减小”或“不变”)。
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(5)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ;ΔH=-192.9kJ/mol
又知H2O(l)= H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
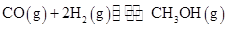 。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
请回答下列问题:
(1)在“图1”中,曲线 (填a或b)表示使用了催化剂;该反应属于 (填吸热、放热)反应。
(2)下列说法正确的是
| A.起始充入的CO为1mol |
| B.增加CO浓度,CO的转化率增大 |
| C.容器中压强恒定时,反应已达平衡状态 |
| D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会减小 |
 CH3OH(g)的化学平衡常数为 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数 (填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数 (填“增大”、“减小”或“不变”)。(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(5)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ;ΔH=-192.9kJ/mol
又知H2O(l)= H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
(1)b 放热 (2)C (3)0.15mol·L-1·min-1 12 减小
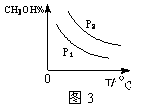
(4)
(5)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-280.9kJ/mol
(4)

(5)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-280.9kJ/mol
试题分析:(1)使用催化剂降低反应活化能,所以是曲线b,由曲线可看出生成物能量不反应物能量低,反应发热。(2)A:CO起始浓度为1mol/L,容器体积2L,故CO起始量应是2mol;B:增加CO浓度,反应速率增大,但转化率不一定增大;(3)根据反应速率计算公式:V(H2)=C(H2)/△t=1.5mol/10min.L=0.15mol·L-1·min-1zai
平衡常数
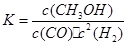 ,代入数据即可算的。该反应属于放热反应,故升高温度反应向左移动,平衡常数减小。(4)反应是放热反应,所以升高温度平衡向左移动,甲醇百分数随温度的升高降低;在相同的温度、体积下,压强越大,单位体积反应物浓度越高,正反应速率加快,平衡向右移动,故甲醇百分数较高,P2在P1之上
,代入数据即可算的。该反应属于放热反应,故升高温度反应向左移动,平衡常数减小。(4)反应是放热反应,所以升高温度平衡向左移动,甲醇百分数随温度的升高降低;在相同的温度、体积下,压强越大,单位体积反应物浓度越高,正反应速率加快,平衡向右移动,故甲醇百分数较高,P2在P1之上点评:综合考查化学平衡章节的内容,熟悉影响化学反应速率及化学平衡的因素及其原理,在此基础上进行推导

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
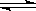 Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26
Fe(s)+ CO2(g) ΔH>0。已知1100℃时,K=0.26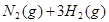
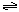
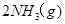
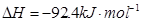 。现
。现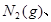 3mol
3mol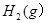 充入一容积为2L的密闭容器中,在500℃下进行反应,10min
充入一容积为2L的密闭容器中,在500℃下进行反应,10min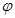 ,下列说法中正确的是( )
,下列说法中正确的是( )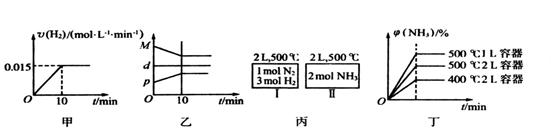
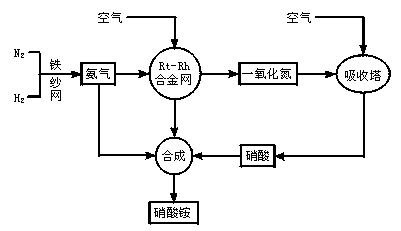
 2NH3(g),Q>0。请解释:
2NH3(g),Q>0。请解释: 2Z(g)+W(s),下列叙述中正确的是
2Z(g)+W(s),下列叙述中正确的是 C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题:
C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题: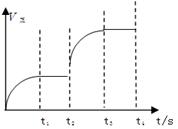
 pC(气)达平衡后,将气体体积缩小到原来的
pC(气)达平衡后,将气体体积缩小到原来的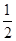 ,当达到新平衡时,C的浓度为原来的1.9倍,其压缩过程中保持温度不变,则反应方程式中两边系数关系是: 。
,当达到新平衡时,C的浓度为原来的1.9倍,其压缩过程中保持温度不变,则反应方程式中两边系数关系是: 。 2C(g),增大压强后,平衡混合气的平均相对分子质量减小
2C(g),增大压强后,平衡混合气的平均相对分子质量减小 bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则 ( )
bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则 ( )