��Ŀ����
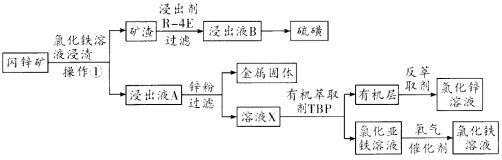
����Ŀ���ס��ҡ������ֻ���������⡢��������ͭ����Ԫ���е�������ɡ������£�����һ�ֺ�����������Ϊ87.5%��Һ̬���������Է��������������ij����Ҫ�ɷֵ���Է���������ȣ��Һͱ���ͭ�����ֳ����������������������ͭ����ȩ��Ӧ�Ļ�ԭ����Իش��������⣺
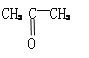
��1���Ľṹʽ ��
��2������һ�ֶ�Ԫ��������������ᷴӦ�IJ���Ϊ (д��ѧʽ)��
��3���ͱ���Ӧ�IJ����к����Һ�һ����̬���ʣ�д���仯ѧ����ʽ ��
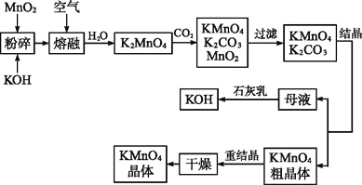
��4�����ҵĹ����м�����������ữ����������Һ���ҹ�����ȫ�ܽ⣬�õ�����Һ��д�������ӷ���ʽ ��
���𰸡���1��![]() ����2��N2H6SO4 ����3��N2H4+4CuO==2Cu2O+N2+2H2O����4����2Fe3++Cu2O+2H+=2Fe2++2Cu2++H2O��
����2��N2H6SO4 ����3��N2H4+4CuO==2Cu2O+N2+2H2O����4����2Fe3++Cu2O+2H+=2Fe2++2Cu2++H2O��
��������
�����������1����������Ҫ�ɷ��ǵ�������������������ֱ�Ϊ28��32����˼������г�N����һ��Ԫ��Ӧ���⣬ϵ����ֵΪ87.5%/14��12.5%/1=1��2�������ʽNH2������Ƿ�����Ϊ28�������ϣ�������Ϊ32����ΪN2H4����ṹʽ��![]() ����2�����NaH4�Ƕ�Ԫ�N2H4��H2SO4=N2H6SO4����3���ס�����ͭ���ֳ��������������������������ͭ����ȩ�ĵĻ�ԭ�������ΪCu2O����ΪCuO��N2H4��CuO��Ӧ�õ�Cu2O��ͭ�Ļ��ϼ۽��ͣ���N�Ļ��ϼ����ߣ���̬����ΪN2����Ӧ����ʽΪN2H4��4CuO=2Cu2O��N2����2H2O����4��Cu2O��Cu���л�ԭ�ԣ�Fe3�����������ԣ����߷���������ԭ��Ӧ��2Fe3����Cu2O��2H��=2Fe2����2Cu2����H2O��
����2�����NaH4�Ƕ�Ԫ�N2H4��H2SO4=N2H6SO4����3���ס�����ͭ���ֳ��������������������������ͭ����ȩ�ĵĻ�ԭ�������ΪCu2O����ΪCuO��N2H4��CuO��Ӧ�õ�Cu2O��ͭ�Ļ��ϼ۽��ͣ���N�Ļ��ϼ����ߣ���̬����ΪN2����Ӧ����ʽΪN2H4��4CuO=2Cu2O��N2����2H2O����4��Cu2O��Cu���л�ԭ�ԣ�Fe3�����������ԣ����߷���������ԭ��Ӧ��2Fe3����Cu2O��2H��=2Fe2����2Cu2����H2O��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�