氨基磺酸(H
2NSO
3H)是一元固体强酸,溶于水和液氨,不溶于乙醇。在工业上用作酸性清洗剂、阻燃剂、磺化剂。用尿素[CO(NH
2)
2]和发烟硫酸(溶有SO
3的硫酸)为原料合成氨基磺酸的路线如下:
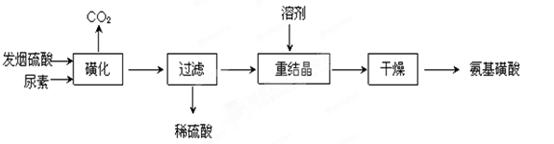
(1)重结晶用10%~12%的硫酸作溶剂而不用水作溶剂的原因是______________
(2)“磺化”步骤中所发生的反应为:
①CO(NH
2)
2(s) + SO
3(g)
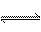
H
2NCONHSO
3H(s) △H<0
②H
2NCONHSO
3H + H
2SO
4
2H
2NSO
3H + CO
2↑
“磺化”过程应控制反应温度为75~80℃,若温度高于80℃,氨基磺酸的产率会降低,原因是_______________ 。
(3)测定产品中氨基磺酸纯度的方法如下:称取7.920g产品配成l000mL待测液,量取25.00mL待测液于锥形瓶中,加入2mL 0.2mol·L
-1稀盐酸,用淀粉碘化钾试剂作指示剂,逐滴加入0.08000mol·L
-1NaNO
2溶液,当溶液恰好变蓝时,消耗NaNO
2溶液25.00mL,此时氨基磺酸恰好被完全氧化成N
2,NaNO
2的还原产物也为N
2。试求产品中氨基磺酸的质量分数
。
(4)以酚酞为指示剂,用NaOH进行酸碱中和滴定也能测定产品中氨基磺酸的纯度,测定结果通常比NaNO
2法偏高,原因是氨基磺酸中混有___________杂质。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案