题目内容
6.氯气在生产生活中应用广泛.(1)多余的氯气可用NaOH溶液吸收,反应的离子方程式为Cl2+2OH?=Cl-+ClO-+H2O.工业上也可用MnSO4溶液吸收氯气,获得Mn2O3,Mn2O3广泛应用于电子工业、印染工业等领域.请写出该化学反应的离子方程式2Mn2++Cl2+3H2O═Mn2O3+6H++2Cl-
(2)海底蕴藏着丰富的锰结核矿,其主要成分是MnO2.1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如图所示:
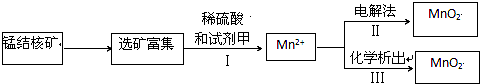
①步骤I中,试剂甲必须具有的性质是B(填序号).
A.氧化性B.还原性C.酸性
②步骤Ⅲ中,以 NaClO 3为氧化剂,当生成0.050mol MnO2时,消耗0.10mol•L-1 的NaClO3溶液200mL,该反应的离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+.
(3)用100mL 12.0mol•L-1的浓盐酸与足量MnO2混合后,加热,反应产生的氯气物质的量远远少于0.30mol,请你分析可能的原因为随着反应的进行,盐酸浓度减小,反应终止.
分析 本题考查氯气的实验室制备原理的分析及用NaOH溶液或MnSO4溶液吸收尾气,另外还探究了MnO2的不同制法,具体是将+2价锰选用氧化剂或通过电解的方法进行氧化得到,重点考查的通过离子方程式讨论反应原理;
(1)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;用MnSO4溶液吸收氯气,获得Mn2O3,是利用氯气在水溶液中氧化硫酸锰为Mn2O3,本身被还原为氯化氢,溶液中生成硫酸,结合质量守恒、电子守恒和电荷守恒可写出此反应的离子方程式;
(2)①步骤I中,Mn元素的化合价由+4价降低为+2价;
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050mol MnO2时,消耗0.10mol•L-1 的NaClO3溶液200mL,利用电子守恒确定还原产物,以此书写离子反应.
(3)根据稀盐酸与二氧化锰不反应进行判断;
解答 解:(1)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,离子反应方程式为Cl2+2OH?=Cl-+ClO-+H2O,MnSO4溶液吸收氯气,生成Mn2O3,氯气被还原为Cl-,离子方程式为 2Mn2++Cl2+3H2O═Mn2O3+6H++2Cl-,
故答案为:Cl2+2OH?=Cl-+ClO-+H2O;2Mn2++Cl2+3H2O═Mn2O3+6H++2Cl-;
(2)①步骤I中,Mn元素的化合价由+4价降低为+2价,则试剂甲应具有还原性,故答案为:B;
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050mol MnO2时,消耗0.10mol•L-1 的NaClO3溶液200mL,设还原产物中Cl的化合价为x,则由电子守恒可知,0.05mol×(4-2)=0.1mol/L×0.2L×(5-x),解得x=0,即生成氯气,则离子反应为2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+,
故答案为:2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+;
(3)用100mL12.0mol•L-1的浓盐酸与足量MnO2混合后,加热,随着反应的进行,盐酸的浓度逐渐降低,还原性逐渐减弱,则生成的氯气的物质的量小于0.30mol,故答案为:随着反应的进行,盐酸浓度减小,反应终止.
点评 本题以氯气及其化合物的性质考查氧化还原反应,明确信息及流流程中Mn元素的化合价变化、电子守恒即可解答,题目难度中等.

| A. | 4 | B. | 6 | C. | 5 | D. | 7 |
| A. | 在碱性溶液中:Na+,NO3-,S2-,SO32- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+,I-,NO3-,Cl- | |
| C. | 碳酸氢钠溶液中:K+,SO42-,Cl-,H+ | |
| D. | 使酚酞试液呈红色的溶液中:Mg2+,Cu2+,SO42-,K+ |
| A. | FeCl2 | B. | Al2S3 | C. | CuCl2 | D. | Mg3N2 |
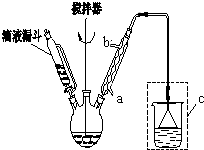 制备水杨酸对正辛基苯基酯(
制备水杨酸对正辛基苯基酯( )如下:
)如下: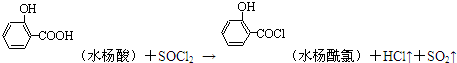
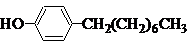 ],温度控制在100℃左右,不断搅拌.
],温度控制在100℃左右,不断搅拌.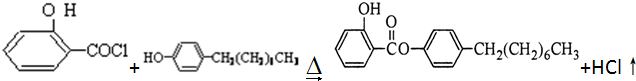 .
.