题目内容
【题目】A、X、W、D、E为短周期元素,且原子序数依次增大。A、D同主族,X、W同周期, X形成的气态氢化物可使湿润的红色石蕊试纸变蓝, A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为______________________。W的原子结构示意图为________。
(2)A、X 两种元素能形成含18电子的分子,请写出该分子的电子式:_______________。
用电子式表示化合物D2W的形成过程______________________________________。
(3)下列事实能说明W元素的非金属性比S元素的非金属性强的是________ (填字母)。
a.W单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol W单质比1 mol S得电子多
c.W和S两元素的简单氢化物受热分解,前者的分解温度高
(4)实验室制备A和X形成的气态化合物的化学方程式为____________________________。
(5)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式_________________________________________________________________________。
(6)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现在改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式________________________________________________________________。
【答案】第三周期 第ⅢA族 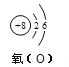
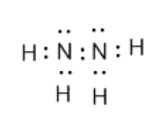
![]() a、c 2NH4Cl+Ca(OH)2
a、c 2NH4Cl+Ca(OH)2![]() CaCl2+2H2O+2NH3↑ H2O2
CaCl2+2H2O+2NH3↑ H2O2![]() H++ HO2- Cu+H2O2+2H+=Cu2+ +2H2O
H++ HO2- Cu+H2O2+2H+=Cu2+ +2H2O
【解析】
根据题干信息判断元素的种类,进而根据元素的性质解题。
A、X、W、D、E为短周期元素,且原子序数依次增大。A、D同主族,X、W同周期, X形成的气态氢化物可使湿润的红色石蕊试纸变蓝,则X为N元素, A、W能形成两种液态化合物A2W和A2W2,则A为H元素,W为O元素,D为Na元素,E元素的周期序数与主族序数相等,则E为Al元素;
(1)Al在元素周期表中的位置为:第三周期 第ⅢA族;O的原子结构示意图为: ;
;
(2)A、X 两种元素能形成含18电子的分子,该分子为N2H4,电子式为: 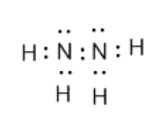 ;
;
用电子式表示氧化钠的形成过程为:![]() ;
;
(3) a.W单质与H2S溶液反应,溶液变浑浊,是因为发生氧化还原反应生成硫单质,单质的氧化性O强于S,非金属性O强于S,故a正确;
b.非金属性强弱是其单质的得电子难易,而不是得电子的数目,故b错误;
c.非金属性越强,其氢化物越稳定,所以W和S两元素的简单氢化物受热分解,前者的分解温度高,能说明W的非金属性强,故c正确;
故选a、c;
(4)实验室制取氨气的方程式为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;
(5)由题中信息可知,双氧水的第一步电离方程式为:H2O2![]() H+ + HO2-;
H+ + HO2-;
(6)双氧水具有氧化性,可以氧化单质铜,该反应的离子方程式为:Cu+H2O2+2H+=Cu2+ +2H2O。

【题目】T1 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1),下列说法错误的是( )
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 2.00 | 3.00 |
t1 | 0.80 | |
t2 | 1.80 |
A. 用H2表示反应在t1 min内的平均速率为v(H2)=0.60/t1mol·L-1·min-1
B. 保持其他条件不变,若起始时向容器中充入3.00 mol CO和2.00 mol H2O(g),达到平衡时,n(CO2)=1.20 mol
C. 保持其他条件不变,在t2 min时向容器中再通入1.00 mol CO,与原平衡相比,达到新平衡时CO转化率将增大
D. 温度升至T2 ℃,上述反应的平衡常数为0.70,则正反应的ΔH<0