题目内容
【题目】已知1-丙醇和2-丙醇的结构简式如下:
1-丙醇:CH3-CH2-CH2-OH
2-丙醇:CH3-![]() -CH3
-CH3
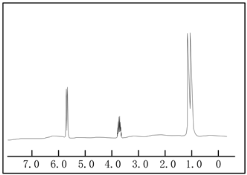
上图是这两种物质的其中一种的核磁共振谱,并且峰面积比分别为1:1:6,请指出该核磁共振谱为何物质,并说明原因_______。
【答案】2-丙醇;有三种峰,且峰面积比为1:1:6,说明有三种不同化学环境的氢原子,且原子个数比为1:1:6,只有2-丙醇符合,而1-丙醇不符合
【解析】
核磁共振谱中的峰面积比分别为1:1:6,说明该有机物分子中含有的不同位置氢原子有3种,分别含有氢原子数之比为1:1:6。
根据该有机物的核磁共振谱中的峰面积比分别为1:1:6可知:该有机物分子中含有的不同位置氢原子有3种,分别含有氢原子数之比为1:1:6,1﹣丙醇(CH3﹣CH2﹣CH2﹣OH}中不同位置的氢原子有四种,其数目之比为1:2:2:3;
2﹣丙醇![]() 中不同位置的氢原子有三种,其氢原子数目之比为1:1:6,所以满足条件的物质为:2﹣丙醇,
中不同位置的氢原子有三种,其氢原子数目之比为1:1:6,所以满足条件的物质为:2﹣丙醇,
故答案为:2-丙醇;有三种峰,且峰面积比为1:1:6,说明有三种不同化学环境的氢原子,且原子个数比为1:1:6,只有2-丙醇符合,而1-丙醇不符合。

【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题:
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是______。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是________。
(3)②③④中形成的简单离子半径由大到小的顺序是________。
(4)元素⑥氢化物常温下和元素②的单质反应的离子方程式是_____________,该氢化物与元素⑧的单质反应的离子方程式是_________________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为________和________。①和⑨两元素形成化合物的化学式为________,该化合物灼烧时焰色为________,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为________。
(7)⑥和⑧形成的化合物的化学式为________,该化合物溶解⑨的单质所得溶液为______________________。
【题目】CoCO3可用作选矿剂、催化剂及伪装涂料的颜料。以含钴废渣(主要成CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
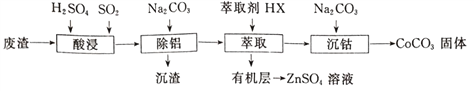
下表是相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算):
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
(1)写出“酸溶”时发生氧化还原反应的化学方程式_________________。
(2)“除铝”过程中需要调节溶液pH的范围为______________,形成沉渣时发生反应的离子方程式为_____________________。
(3)在实验室里,萃取操作用到的玻璃仪器主要有____________;上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ![]() ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是_________________________。
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是_________________________。
(4)“沉钴”时,Na2CO3溶液滴加过快会导致产品不纯,请解释原因_________________。
(5)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为____________________。