题目内容
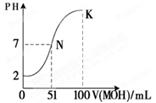
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
| A.c(NH4+)>c(Cl-)>c(OH-)>c(H+) | B.c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D.c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
② 若为HCl 和NH4Cl 混合溶液,则四种离子浓度的由大到小的顺序是_________;
若为NH3· H2O 和NH4Cl 混合溶液,四种离子浓度的由大到小的顺序是__________。
③ 若该溶液是由体积相等的HCl溶液和氨水混合而成,且恰好呈中性,则混合前c(HCl) _____c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(OH-)____c(NH4+)。
(1)C (2)B; A (3) <; <
解析试题分析:① 若为NH4Cl 溶液,由于NH4+水解消耗水电离产生的OH-离子,所以这四种离子浓度的由大到小的顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-)。选项为:C。② 由于溶液中的Cl-由HCl 和NH4Cl共同电离产生,所以,溶液中的H+有酸的电离、NH4+的水解产生,所以c(H+)>c(NH4+);盐水解的程度很微弱,故c(NH4+)>c(OH-)。因此在HCl 和NH4Cl 混合溶液中四种离子浓度的由大到小的顺序是c(Cl-)>c(H+)>c(NH4+)>c(OH-)。选项为:B。若为NH3· H2O 和NH4Cl 混合溶液,由于NH3· H2O的电离作用大于NH4+水解作用。C(NH4+)>c(Cl-),c(OH-)>c(H+)。盐的电离远大于水的电离,所以c(Cl-) >c(OH-)。故再此混合溶液,四种离子浓度的由大到小的顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+)。选项为:A.③ 若该溶液是由体积相等的HCl溶液和氨水混合而成,且恰好呈中性,则c(NH4+)=c(Cl-),c(OH-)=c(H+)。由于HCl为强酸,完全电离,NH3·H2O为弱碱,部分电离,所以要保证混合后溶液呈中性,n(NH3·H2O) >n(HCl).即混合前c(HCl) <c(NH3·H2O)。混合后溶液中盐电离产生的NH4+比水电离产生的OH-物质的量要多。故c(OH-) <c(NH4+)。
考点:考查存在相同种类的离子的溶液中由于离子的相对量的多少不同,所含有的溶质不同的情况的知识。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案硫元素的含氧酸盐在工业上用途广泛,完成下列填空。
工业上用Na2SO3溶液处理工业尾气中的SO2,下表数据表示反应过程中 随pH变化的关系:
随pH变化的关系:
 | 91:9 | 1:1 | 9:91 |
| 室温下pH | 8.2 | 7.2 | 6.2 |
(1)简述
 = 1时,溶液pH= 7.2的原因:___________________;若用0.20 mol/L 的NaOH溶液(反应前后溶液体积不变)吸收SO2,若反应后溶液呈中性,则
= 1时,溶液pH= 7.2的原因:___________________;若用0.20 mol/L 的NaOH溶液(反应前后溶液体积不变)吸收SO2,若反应后溶液呈中性,则c (HSO3-) + 2c (SO32-) =" _______" mol/L 。
(2)已知:Ki1(H2SO3)> Ki(HAc) > Ki2(H2SO3) > Ki2(H2CO3),要使NaHSO3溶液中c(Na+):c(HSO3-)接近1:1,可在溶液中加入少量____________。
a.H2SO3溶液 b.NaOH溶液 c.冰醋酸 d.Na2CO3
(3)实验室通过低温电解KHSO4溶液制备过二硫酸钾K2S2O8,写出熔融KHSO4的电离方程式:__________________________________________。
(4)S2O82-有强氧化性,还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。书写此反应的化学方程式: 。
(5)已知:S2O32-有较强的还原性,实验室可用I-测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2 ……① I2+2S2O32-→2I-+S4O62-……②
S2O82-、S4O62-、I2氧化性强弱顺序:__________________________。
(6)K2S2O8是偏氟乙烯(CH2=CF2)聚合的引发剂,偏氟乙烯由CH3—CClF2气体脱去HCl制得,生成0.5 mol偏氟乙烯气体要吸收54 kJ的热,写出反应的热化学方程式_______。
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)写出醋酸的电离方程式: 。
(2)醋酸溶液中存在的微粒有 。
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是 。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度(填增大、减小或不变) 。
胆矾是一种常见的化合物,工业上它也是一种制取其它含铜化合物的原料,现有废铜(主要杂质为Fe)来制备胆矾。有人设计了如下流程: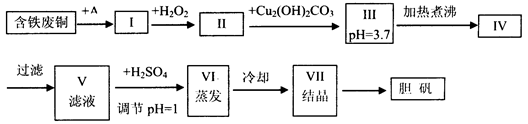
pH值控制可参考下列数据
| 物质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
请根据上述流程回答下列问题:
(1)A可选用________(填字母)
a.稀H2SO4 b.浓H2SO4、加热 c.浓FeCl3溶液 d.浓HNO3
(2)Ⅰ中加H2O2的目的___________________________________________________。
(3)Ⅱ中加Cu2(OH)2CO3的目的是___________________________________,
其优点是_____________________________________________________________。
(4)Ⅲ加热煮沸时发生的化学反应的离子方程式为___________________________。
(5)V中加H2SO4调节pH=1是为了_________________________________________,
某工程师认为上述流程中所加的A物质并不理想,需作改进,其理由是______________,
若你是工程师,将对所加的A物质作何改进?请提出建议______________________。
 CH3COO-+H+ ΔH>0
CH3COO-+H+ ΔH>0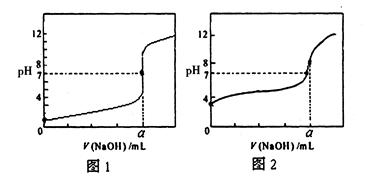
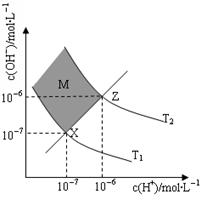
 mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。