题目内容
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是AgNO3,则在银电极上析出______单质;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极(从铜、银中选填.)
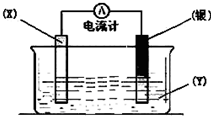
(1)电极X的材料是______;电解质溶液Y是AgNO3,则在银电极上析出______单质;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极(从铜、银中选填.)

(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,Ag+在正极上得电子被还原,在银电极上析出Ag单质,
故答案为:Cu;Ag;
(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e-=Ag,而负极反应为Cu-2e-=Cu2+,
故答案为:正;Ag++e-=Ag; Cu-2e-=Cu2+;
(3)原电池中,电子从负极经外电路流向正极,本题中由Cu极经外电路流向Ag极,故答案为:Cu;Ag.
故答案为:Cu;Ag;
(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e-=Ag,而负极反应为Cu-2e-=Cu2+,
故答案为:正;Ag++e-=Ag; Cu-2e-=Cu2+;
(3)原电池中,电子从负极经外电路流向正极,本题中由Cu极经外电路流向Ag极,故答案为:Cu;Ag.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
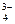 +2I—+2H+
+2I—+2H+  AsO
AsO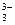 +I2+H2O设计成右下图所示的电化学装置,其中C1、C2均为碳棒。甲、乙两组同学分别进行下述操作(盐桥能能让离子通过):
+I2+H2O设计成右下图所示的电化学装置,其中C1、C2均为碳棒。甲、乙两组同学分别进行下述操作(盐桥能能让离子通过):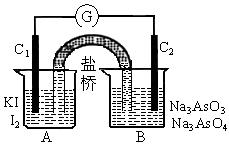
 2H2O
2H2O 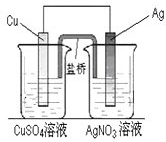
 CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①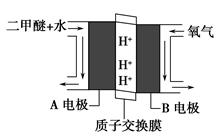
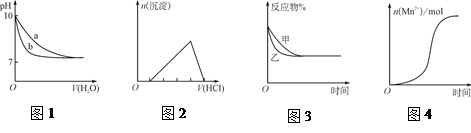
 CO2(g)+H2(g)的影响,乙的压强比甲的压强大
CO2(g)+H2(g)的影响,乙的压强比甲的压强大 H2NCOONH4(氨基甲酸铵)(l) △H1
H2NCOONH4(氨基甲酸铵)(l) △H1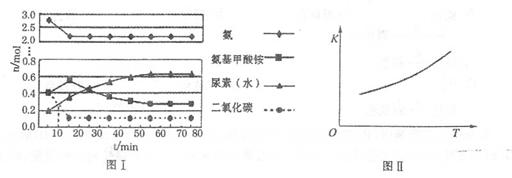
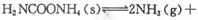
 。实验测得不同温度下的平衡数据列于下表:
。实验测得不同温度下的平衡数据列于下表: