题目内容
10. 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法错误的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法错误的是( )| A. | 该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 | |
| B. | 取10 mL该硫酸于烧杯中,再加18.4 mL的水,可配得49%的硫酸 | |
| C. | 配制200 mL 4.6 mol•L-1的稀硫酸需取该硫酸50 mL | |
| D. | 该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol•L-1 |
分析 A.98%的硫酸为浓硫酸,具有强腐蚀性;
B.硫酸的密度大于水,等体积时硫酸溶液的质量大;
C.根据c=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,根据溶液稀释前后溶质的物质的量不变计算;
D.硫酸与等质量的水混合所得溶液的体积大于硫酸体积的2倍.
解答 解:A.98%的硫酸为浓硫酸,具有强腐蚀性,属于危险药品,在实验室中应妥善保管,故A正确;
B.硫酸的密度大于水,等体积时硫酸溶液的质量大,所配溶液的质量分数大于49%,故B错误;
C.该浓硫酸的物质的量浓度为c═$\frac{1000ρω}{M}$=$\frac{1000×1.84g/L×98%}{98g/mol}$=18.4mol/L,计算根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则xmL×18.4mol/L=200mL×4.6mol/L,解得:x=50,所以应量取的浓硫酸体积是50mL,故C正确;
D.该硫酸与等质量的水混合,由于硫酸密度大于水的密度,等质量混合时总体积大于硫酸体积的2倍,则所得溶液的物质的量浓度小于9.2 mol•L-1,故D正确;
故选B.
点评 本题考查物质的量浓度的计算,题目难度中等,注意硫酸密度比水大的特点,答题中注意把握相关计算公式的运用,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
20.X、Y、Z、W、R是五种常见的前四周期元素,原子序数依次增大,其相关信息如下表:
(1)元素W在周期表中的位置是第三周期,第ⅥA族,R基态原子的价电子排布式为3d54s1.
(2)Y的电离能比X的小(填“大”或“小”),Y的最简单氢化物由液态变为气态所需克服的微粒间作用力是氢键;
(3)ZX3受撞击会产生一种离子化合物和一种气态单质,该反应的化学方程式是3NaN3=Na3N+4N2↑.
(4)工业废水中含有的R2O72-离子,常用Fe2+将其还原为R3+离子,再通过调节溶液的pH值,使其转化为
氢氧化物沉淀除去.试写出酸性条件下R2O72-与Fe2+反应的离子方程式:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
(5)已知在25℃、101KPa时:2Cu(s)+W(s)=Cu2W(s)△H=-79.5KJ/mol
W(s)+Y2(g)=WY2(g)△H=-296.6KJ/mol
根据上述反应,请写出Cu2W与Y2反应生成Cu与WY2的热化学方程式Cu2S(s)+O2(g)=2Cu(s)+SO2(g)△H=-217.1KJ/mol.
| 元素 | 相关信息 |
| X | X单质分子中σ键和π键数目之比为1:2 |
| Y | Y 基态原子的最外层电子排布式为 nsnnpn+2 |
| Z | Z的第一电离能在同周期主族元素中最小 |
| W | W的氧化物是导致酸雨的主要物质之一 |
| R | 基态原子的核外电子排布中未成对的电子数最多 |
(2)Y的电离能比X的小(填“大”或“小”),Y的最简单氢化物由液态变为气态所需克服的微粒间作用力是氢键;
(3)ZX3受撞击会产生一种离子化合物和一种气态单质,该反应的化学方程式是3NaN3=Na3N+4N2↑.
(4)工业废水中含有的R2O72-离子,常用Fe2+将其还原为R3+离子,再通过调节溶液的pH值,使其转化为
氢氧化物沉淀除去.试写出酸性条件下R2O72-与Fe2+反应的离子方程式:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
(5)已知在25℃、101KPa时:2Cu(s)+W(s)=Cu2W(s)△H=-79.5KJ/mol
W(s)+Y2(g)=WY2(g)△H=-296.6KJ/mol
根据上述反应,请写出Cu2W与Y2反应生成Cu与WY2的热化学方程式Cu2S(s)+O2(g)=2Cu(s)+SO2(g)△H=-217.1KJ/mol.
1.下列有关化学用语表示正确的是( )
| A. | Na2O2的电子式为 | B. | NH4Br的电子式: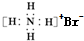 | ||
| C. | 氢氧根离子的电子式: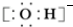 | D. | HClO的电子式: |
18.最简式相同,既不是同系物,又不是同分异构体的是( )
| A. | 1辛烯和3甲1丁烯 | B. | 苯和乙炔 | ||
| C. | 正丁烷和2甲基丙烷 | D. | 甲苯和乙苯 |
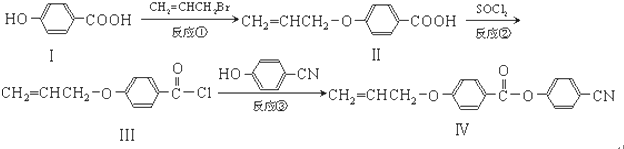
 .
.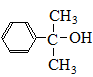 也可与Ⅲ发生类似反应③的反应,生成有机物V,V的结构简式是
也可与Ⅲ发生类似反应③的反应,生成有机物V,V的结构简式是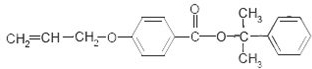 .
.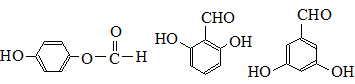 (任写一种).
(任写一种).
 .
.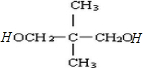 .
.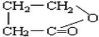 .
.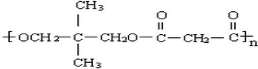 .
.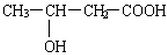 、
、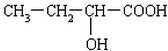 、
、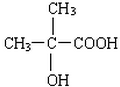 、
、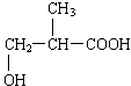 .
.