题目内容
19.下列叙述正确的是( )①任何化学反应都有反应热
②化合物MgO、SiO2、Al2O3中化学键的类型相同
③有些化学键断裂时吸收能量,有些化学键断裂时放出能量
④PH3分子稳定性和沸点均低于NH3分子
⑤O3和NO2都是共价化合物
⑥有热量变化的过程一定有化学键的断裂与形成
⑦单质中不可能有离子键
⑧有化学键断裂的变化属于化学变化.
| A. | ①④⑦ | B. | ②③ | C. | ③⑤ | D. | ②⑤⑥ |
分析 ①化学反应中断键吸收能量,成键放出能量;
②活泼金属与活泼非金属之间形成离子键,非金属之间形成共价键;
③断键吸收能量,成键放出能量;
④非金属性越强,其氢化物越稳定,分子间存在氢键的沸点较高;
⑤只含有共价键的化合物是共价化合物;
⑥物理变化过程中可能存在热效应;
⑦含有离子键的物质属于离子化合物;
⑧有旧化学键断裂和新化学键的生成的变化属于化学变化.
解答 解:①化学反应中断键吸收能量,成键放出能量,所以任何化学反应都有反应热,故正确;
②活泼金属与活泼非金属之间形成离子键,非金属之间形成共价键,MgO、Al2O3中存在离子键,SiO2中存在共价键,所以化学键的类型不相同,故错误;
③断键吸收能量,成键放出能量,所以化学键断裂时不能放出能量,故错误;
④非金属性越强,其氢化物越稳定,则PH3分子稳定性均低于NH3分子,分子间存在氢键的沸点较高,氨气分子间有氢键,所以PH3分子沸点低于NH3分子,故正确;
⑤只含有共价键的化合物是共价化合物,NO2是共价化合物,O3是单质,故错误;
⑥物理变化过程中可能存在热效应,如浓硫酸稀释属于物理变化,过程中会放出热量,故错误;
⑦含有离子键的物质属于离子化合物,单质中没有离子键,故错误;
⑧有旧化学键断裂和新化学键的生成的变化属于化学变化,有化学键断裂的变化不一定属于化学变化,如HCl溶于水,H-Cl键断裂,属于物理变化,故错误.
故选A.
点评 本题考查了化学反应中的能量变化、化学键、元素周期律、共价化合物和离子化合物等,题目涉及的知识点较多,侧重于基础知识的综合应用能力的考查,但是难度不大.

练习册系列答案
相关题目
10.药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:下列有关叙述正确的是( )
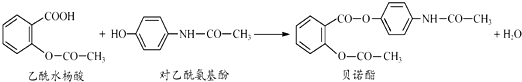

| A. | 贝诺酯分子中有三种含氧官能团 | |
| B. | 用FeCl3 溶液不能区别乙酰水杨酸和对乙酰氨基酚 | |
| C. | 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3 溶液反应 | |
| D. | 1mol贝诺酯与足量NaOH 溶液共热最多可消耗5molNaOH钠 |
7.下列有关化学键的叙述,正确的是( )
| A. | 非金属元素组成的化合物中只含共价键 | |
| B. | 水溶液能导电的化合物一定是离子化合物 | |
| C. | 化合物MgO、SiO2、SO3中化学键的类型相同 | |
| D. | PH3分子稳定性低于NH3分子,因为N-H键键能高 |
4.室温下,下列溶液中粒子浓度关系正确的是( )
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O${\;}_{4}^{-}$)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO${\;}_{3}^{2-}$)+c(OH-) | |
| D. | CH3COONa溶液:c(Na+)>c(CH3COO-) |
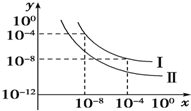 在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸: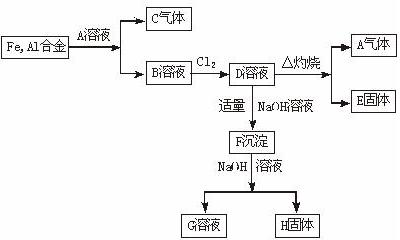 从铁、铝合金出发的反应如图所示:
从铁、铝合金出发的反应如图所示: