题目内容
准确称取6.0 g铝土矿样品(含Fe2O3),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如右图所示。则所用硫酸物质的量浓度为
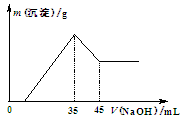

| A.1.75 mol·L-1 | B.3.50 mol·L-1 | C.0.85 mol·L-1 | D.无法确定 |
A
当加入NaOH溶液的体积为35ml时,n(NaOH)=0.035L×10mol/L=0.35mol,
此时沉淀的质量达到最大值,则此时溶液的溶质只有Na2SO4,
根据Na元素守恒,
则有:n(H2SO4)=n(Na2SO4)=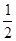 n(NaOH)=
n(NaOH)=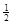 ×0.35mol=0.175mol,
×0.35mol=0.175mol,
c(H2SO4)="0.175mol/" 0.1L =1.75mol/L,
故选A
点评:本题考查物质的量浓度的计算,题目难度中等,本题做题时根据反应判断沉淀最大值时,溶液的溶质,结合质量守恒计算,可省去中间繁杂的计算过程.
此时沉淀的质量达到最大值,则此时溶液的溶质只有Na2SO4,
根据Na元素守恒,
则有:n(H2SO4)=n(Na2SO4)=
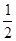 n(NaOH)=
n(NaOH)=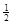 ×0.35mol=0.175mol,
×0.35mol=0.175mol,c(H2SO4)="0.175mol/" 0.1L =1.75mol/L,
故选A
点评:本题考查物质的量浓度的计算,题目难度中等,本题做题时根据反应判断沉淀最大值时,溶液的溶质,结合质量守恒计算,可省去中间繁杂的计算过程.

练习册系列答案
相关题目