题目内容
12.现有下列4种有机物:①乙炔、②甲苯、③苯酚、④溴乙烷.请回答:(1)能发生消去反应生成乙烯的是④(填序号).
化学方程式CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O
(2)能发生加成反应生成氯乙烯的是①(填序号).
化学方程式CH≡CH+HCl$\stackrel{催化剂}{→}$CH2=CHCl
(3)能与饱和溴水反应产生白色沉淀的是③(填序号).
化学方程式

(4)能与硝酸反应制烈性炸药TNT的是②(填序号).
化学方程式
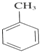 +3HNO3$\stackrel{浓硫酸}{→}$
+3HNO3$\stackrel{浓硫酸}{→}$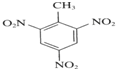 +3H2O.
+3H2O.
分析 (1)溴乙烷含有Br,可在氢氧化钠醇溶液中加热条件下发生消去反应;
(2)乙炔含有C≡C键,可与HCl发生加成反应生成氯乙烯;
(3)苯酚可与溴水发生取代反应生成三溴苯酚白色沉淀;
(4)甲苯可与硝酸反应制烈性炸药TNT.
解答 解:(1)溴乙烷含有Br,可在氢氧化钠醇溶液中加热条件下发生消去反应,方程式为CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O,
故答案为:④;CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O;
(2)乙炔含有C≡C键,可与HCl发生加成反应生成氯乙烯,方程式为CH≡CH+HCl$\stackrel{催化剂}{→}$CH2=CHCl,故答案为:①;CH≡CH+HCl$\stackrel{催化剂}{→}$CH2=CHCl;
(3)苯酚与浓溴水反应,是苯酚分子中羟基对苯环影响,邻对位氢原子活泼,易于发生取代反应,反应的化学方程式为: ,
,
故答案为:③; ;
;
(4)甲苯可与硝酸反应制烈性炸药TNT,方程式为 +3HNO3$\stackrel{浓硫酸}{→}$
+3HNO3$\stackrel{浓硫酸}{→}$ +3H2O,
+3H2O,
故答案为:②; +3HNO3$\stackrel{浓硫酸}{→}$
+3HNO3$\stackrel{浓硫酸}{→}$ +3H2O.
+3H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重甲苯、苯酚、乙炔性质的考查,题目难度不大.

练习册系列答案
相关题目
2.同温同压下,对下列气体叙述不正确的是( )
| A. | 8gO2和1gH2体积为1:2 | B. | NH3和H2S密度比为1:2 | ||
| C. | 5L N2和4L CH4原子数比为1:2 | D. | 2mol CO2和1mol CO分子数比为2:1 |
3.高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=a kJ•mol-1.
(1)已知:①Fe2O3(s)+3C(石墨,s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
②C(石墨,s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1
则a=-28.5.
(2)冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L的恒容密闭容器甲和乙中,分别按如表所示数据加入物质,反应经10分钟后达到平衡.
①甲容器中:CO的平衡转化率为60%,反应从开始到平衡CO2平均反应速率=0.03mol/(L.min).
②下列说法正确的是abc(填字母).
a.容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙两容器中,CO的平衡浓度之比为2:3
d.增加Fe2O3的量可以提高CO的转化率.
(1)已知:①Fe2O3(s)+3C(石墨,s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
②C(石墨,s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1
则a=-28.5.
(2)冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L的恒容密闭容器甲和乙中,分别按如表所示数据加入物质,反应经10分钟后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
②下列说法正确的是abc(填字母).
a.容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙两容器中,CO的平衡浓度之比为2:3
d.增加Fe2O3的量可以提高CO的转化率.
20.下列溶液中,跟100mL 1.0mol•L -1AlCl3溶液所含的Cl-物质的量浓度相同的是( )
| A. | 100mL 0.5 mol•L-1MgCl2溶液 | B. | 200mL 1.5 mol•L-1CaCl2溶液 | ||
| C. | 50mL 1 mol•L-1NaCl溶液 | D. | 25mL 0.5 mol•L-1vHCl溶液 |
17.有一种生产碘的方法是用Na2SO3还原碘酸盐(IO3-),每还原出2mol I2,理论上需用去Na2SO3( )
| A. | 2mol | B. | 4mol | C. | 5mol | D. | 10mol |
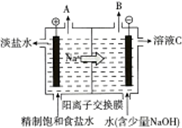 电解饱和食盐水的原理如图所示.
电解饱和食盐水的原理如图所示.