题目内容
1.如图所示,A、B、C三个装置中的三个烧杯分别盛有足量的CuCl2溶液.
(1)A池中Zn是负极,A中总反应的化学方程式为Zn+CuCl2=Cu+ZnCl2.
(2)B池是电解池,C极发生还原反应,反应一段时间Pt极质量不变(填“增加”、“减少”或“不变”).
(3)C池中Cu极的电极反应式为Cu-2e-=Cu2+.反应过程中,CuCl2溶液浓度不变(填“增加”、“减少”或“不变”).
分析 (1)铜、锌、氯化铜原电池中,较活泼的金属作负极,负极上失电子发生氧化反应,较不活泼的金属作正极,正极上得电子发生还原反应,将正负极电极反应式相加即得电池反应式;
(2)该装置是电解池,连接电源负极的是阴极,阴极上得电子发生还原反应,连接电源正极的是阳极,阳极上失电子发生氧化反应;
(3)该装置是电解池,阳极上活泼金属,所以阳极上金属失电子发生氧化反应,正极上阴离子得电子发生还原反应,根据阴阳极上的电极反应式确定溶液浓度是否变化.
解答 解:(1)铜、锌、氯化铜原电池中,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+,铜作正极,正极上铜离子得电子发生还原反应,电极反应式为:Cu2++2e-=Cu,所以该原电池的电池反应式为:Zn+CuCl2=Cu+ZnCl2,
故答案为:负;Zn+CuCl2=Cu+ZnCl2;
(2)该装置是电解池,且阳极是惰性电极,C连接电源负极,所以是阴极,阴极上铜离子得电子发生还原反应,电极反应式为:Cu2++2e-=Cu,铂连接电源正极,所以铂在阳极,阳极上氯离子失电子发生氧化反应,电极反应式为:2Cl--2e-=Cl2↑,所以反应一段时间Pt极质量不变,
故答案为:电解;还原;不变;
(3)该装置是电解池,且阳极是活泼电极,锌是阴极,阴极上铜离子得电子发生还原反应,电极反应式为:Cu2++2e-=Cu,铜是阳极,阳极上铜失电子发生氧化反应,电极反应式为:Cu-2e-=Cu2+,阴极上析出的铜恰好等于阳极上溶解的铜,所以溶液中浓度不变,
故答案为:Cu-2e-=Cu2+;不变.
点评 本题考查原电池和电解池原理,易错题是(3),注意电解池中,活泼电极作阳极,则阳极上电极材料失电子而不是电解质溶液中阴离子失电子,为易错点.

| A. | 酒精在实验台上燃烧时,用水扑灭火焰 | |
| B. | 给试管中的液体加热,试管口不能对着人 | |
| C. | 在烧杯中稀释浓硫酸时,应将水慢慢注入浓硫酸中,并用玻璃棒搅拌 | |
| D. | 不慎将浓硫酸沾到皮肤上,用干抹布擦净即可 |
| A. | 溴苯中含有溴单质,可用NaOH溶液洗涤,再经分液而除去 | |
| B. | 除去苯中的少量苯酚:加入NaOH溶液、振荡、静置分层后,除去水层 | |
| C. | 除去乙酸乙酯中少量的乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯 | |
| D. | 用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀 |
| A. | 甲烷分子中4个氢原子可能在同一平面上 | |
| B. | 乙烯分子中共6个原子都在同一平面上 | |
| C. | 苯分子中碳原子和全部氢原子不可能在同一平面上 | |
| D. | 乙炔分子中4个原子不可能在同一条直线上 |
| A. | n (NH3•H2O) | B. | n (OH-) | C. | c (NH3•H2O) | D. | c (NH4+) |
| 温度/℃ | 700 | 800 | 900 |
| 平衡常数 | 0.1 | X | 1 |
| A. | △H>0 | |
| B. | 平衡时,c(B)为0.6 mol•L-1 | |
| C. | 800℃时平衡常数X=4/9 | |
| D. | 900℃该反应达到平衡状态时,A的物质的量为0.5 mol |
| A. | 大理石上滴加稀盐酸:CO${\;}_{3}^{2-}$+2H+═H2O+CO2↑ | |
| B. | 铁片加入稀H2SO4中:2Fe+6H+=═2Fe3++3H2↑ | |
| C. | NaHSO4溶液与BaCl2溶液混合:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| D. | 稀H2SO4和Ba(OH)2溶液混合:Ba2++H++OH-+SO${\;}_{4}^{2-}$═BaSO4↓+H |
| A. | 4.2×10-10mol•L-1 | B. | 8.4×10-10mol•L-1 | ||
| C. | 3.1×10-10mol•L-1 | D. | 5.8×10-10mol•L-1 |

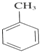 +3HNO3$\stackrel{浓硫酸}{→}$
+3HNO3$\stackrel{浓硫酸}{→}$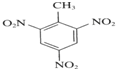 +3H2O.
+3H2O.