题目内容
【题目】已知Ⅰ容器恒压,Ⅱ容器恒容,其它条件相同时,在Ⅰ、Ⅱ中分别加入3mol Z,起始时容积相同,发生反应2X(g)+2Y(s)3Z(g)并达平衡。下列说法正确的是( )

A.从起始到平衡所需时间:Ⅰ>Ⅱ
B.平衡后若在Ⅱ中再加入2molZ,则新平衡时Z的体积分数变小
C.平衡时Z的转化率:Ⅰ<Ⅱ
D.平衡后若在Ⅰ中再加入0.1molY,则X的物质的量将减少
【答案】B
【解析】
在Ⅰ、Ⅱ中分别加入3mol Z,起始时容积相同,发生反应3Z(g) 2X(g)+2Y(s)并达平衡;正反应是气体体积减小的反应,虽然反应的进行,压强减小,Ⅰ容器为恒压,体积减小,相比于Ⅱ,压强增大,平衡正向移动程度更大。
在Ⅰ、Ⅱ中分别加入3mol Z,起始时容积相同,发生反应3Z(g) 2X(g)+2Y(s)并达平衡;
A、该反应正反应是气体物质的量减小的反应,I是恒压密闭容器,II是恒容密闭容器,反应Ⅰ压强大于反应Ⅱ压强,压强增大,反应速率加快,则从起始到平衡所需时间:Ⅰ<Ⅱ,故A错误;
B、平衡后若在Ⅱ中再加入2molZ ,相当于在原来基础上缩小体积,压强增大,则平衡正向移动,则新平衡时Z的体积分数变小,故B正确;
C、反应Ⅰ压强大于反应Ⅱ压强,压强增大平衡向正反应移动,则平衡时Z的转化率: Ⅰ>Ⅱ,故C错误;
D、Y为固体,增大Y的量,不影响平衡移动,则X的物质的量不变,故D错误;
故答案选B。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案【题目】某化学兴趣小组拟用右图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁屑、稀硫酸、氢氧化钠溶液。
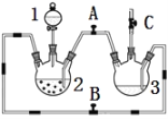
(1)稀硫酸应放在中___(填写仪器名称).
(2)本实验通过控制A、B、C三个开关将仪器中的空气排尽后,再关闭开关___、打开开关___,就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由___。
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是___。
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为了洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是___
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
Ⅰ.滴定过程中发生反应的离子方程式为___。
Ⅱ.上表中第一次实验中记录数据明显大于后两次,其原因可能是___(填字母代号)。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴无气泡,滴定结束有气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
Ⅲ.通过实验数据计算的该产品纯度为___(用字母a、c表示)。
【题目】I:电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25 ℃):
化学式 | 电离平衡常数 |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1)25 ℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为______(填写序号)
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的离子方程式为__________;
(3)现有浓度为0.02 mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是____(填标号)。
A.c(H+)>c(OH-) B.c(H+)<c(OH-)
C.c(H+)+c(HCN) = c(OH-) D.c(HCN)+ c(CN-)=0.01mol/L
(4)已知NaHCO3溶液呈碱性,原因是____(用离子方程式表示);请写出该溶液中各离子浓度的大小_____________,电荷守恒表达式_________;
II:按要求填空:
(1)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的____________。
(2)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理_______;
(3)将25℃下pH=12的NaOH溶液aL与pH=1的HCl溶液b L混合,若所得混合液为中性,则a:b=_____。(溶液体积变化忽略不计)。