题目内容
9.下列有关物质的性质和该性质的应用均正确的是( )| A. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| B. | 油脂在碱性条件下易水解,可用于制作肥皂 | |
| C. | 次氯酸钠具有强还原性,可用于配制“84”消毒液 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
分析 A.氨气和水反应生成一水合氨,一水合氨电离生成氢氧根离子而导致氨水呈碱性,氯化铁和一水合氨反应生成氢氧化铁沉淀;
B.油脂在碱性条件下水解生成高级脂肪酸钠和甘油;
C.次氯酸钠具有强氧化性,能杀菌消毒;
D.常温下,铝和浓硝酸发生钝化现象.
解答 解:A.氨气和水反应生成一水合氨,一水合氨电离生成氢氧根离子而导致氨水呈碱性,氯化铁和一水合氨反应生成氢氧化铁沉淀,应该将几滴氯化铁溶液加入到沸水中制取氢氧化铁胶体,故A错误;
B.油脂在碱性条件下水解生成高级脂肪酸钠和甘油,高级脂肪酸钠是肥皂的成分,故B正确;
C.次氯酸钠具有强氧化性,能杀菌消毒,所以次氯酸钠用于配制“84”消毒液,故C错误;
D.常温下,铝和浓硝酸发生钝化而阻止进一步被氧化,该现象为钝化现象,所以常温下可以用Al运输浓硝酸,常温下铜和浓硝酸反应生成可溶性的硝酸铜,所以不能用铜代替铝,故D错误;
故选B.
点评 本题考查较综合,涉及氢氧化铁胶体制备、油脂的水解、次氯酸钠的运用、钝化现象等知识点,明确反应原理是解本题关键,注意D中Al不是和浓硝酸不反应,为易错点.

练习册系列答案
相关题目
19.下列叙述正确的是( )
| A. | 原子晶体中只存在非极性共价键 | |
| B. | 甲烷?氨和水都是由极性键结合而成的极性分子 | |
| C. | 金属晶体的熔点一定比原子晶体低,比分子晶体高 | |
| D. | H2O的沸点比H2S高,是因为H2O分子间存在氢键 |
20.对有机物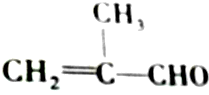 的化学性质叙述错误的是( )
的化学性质叙述错误的是( )
 的化学性质叙述错误的是( )
的化学性质叙述错误的是( )| A. | 既能发生氧化反应,又能发生还原反应 | |
| B. | 1 mol该物质只能与1 mol Br2发生加成反应 | |
| C. | 能发生加聚反应 | |
| D. | 能将新制的Cu(OH)2氧化 |
14.伞形酮可用作荧光指示剂和酸碱指示剂.其合成方法为:
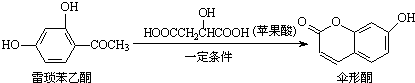
下列有关这三种物质的说法正确的是( )
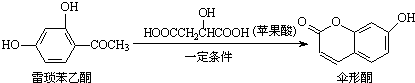
下列有关这三种物质的说法正确的是( )
| A. | 雷琐苯乙酮所有碳原子不可能共平面 | |
| B. | 雷琐苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应 | |
| C. | 1 mol雷琐苯乙酮跟足量H2反应,最多消耗3 mol H2 | |
| D. | 1 mol伞形酮与足量NaOH溶液反应,最多消耗3 mol NaOH |
3.相同条件下,将1体积的CO和2体积的CO2混合,混合气体中碳、氧原子个数之比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 3:5 |
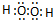 .
.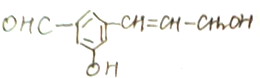 在下列反应中生成的有机物的结构简式.
在下列反应中生成的有机物的结构简式.