题目内容
8.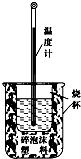 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题:(1)该图中有两处未画出,它们是环形玻璃搅拌棒、烧杯上方盖硬纸板.
(2)如果用0.50mol•L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的热值将偏大(填“偏大”、“偏小”或“不变”);原因是氢氧化钠固体溶于水放热.
分析 (1)根据量热计的构造来判断该装置的缺少仪器;根据中和热测定实验成败的关键是保温工作;
(2)氢氧化钠固体溶于水放出热量.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,为了减少热量的损失,烧杯上方盖硬纸板;
故答案为:环形玻璃搅拌棒;烧杯上方盖硬纸板;
(2)氢氧化钠固体溶于水放热,反应后温度偏高,计算所得热量偏大,所以实验中测得的“中和热”数值将偏大;
故答案为:偏大;氢氧化钠固体溶于水放热.
点评 本题考查学生中和热测定,保温工作是实验成功的关键,可以根据所学内容来回答,难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
18.2003年6月21日,考古专家在西安清理一件刚刚从古墓中出土的西汉早期凤首铜钟时,发现其中盛放着10余斤青绿色的米酒,香味仍然扑鼻.这种香味是由哪种物质引起的( )
| A. | 乙酸乙酯 | B. | 乙酸 | C. | 乙醇 | D. | 乙醛 |
19.分子式为C7H16的化合物,共有几种不同的结构( )
| A. | 10种 | B. | 9种 | C. | 8种 | D. | 7种 |
16.将浓度均为0.1mol/L的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是( )
| A. | BaCl2 NaOH NaHCO3 | B. | AlCl3 NH3•H2O NaOH | ||
| C. | Ba(OH)2 CaCl2 Na2SO4 | D. | Na2CO3 MgCl2 H2SO4 |
3.下列有关胶体的说法正确的是( )
| A. | 分散质粒子直径介于10-9 m~10-7m之间的分散系称为胶体 | |
| B. | 电泳现象可证明胶体带有电荷 | |
| C. | 用聚光手电筒照射FeCl3溶液和Fe(OH)3胶体时,产生的现象相同 | |
| D. | Fe(OH)3难溶于水,因此可以用向煮沸的氢氧化钠溶液中滴加饱和三氯化铁溶液的方法制备氢氧化铁胶体 |
13.下列表示物质结构的化学用语或模型图正确的是( )
| A. | 14C的原子结构示意图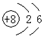 | B. | H2O2的电子式: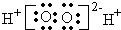 | ||
| C. | CO2的比例模型: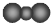 | D. | HClO的结构式:H-O-Cl |
17.下列有机物属于芳香族化合物的是( )
| A. | 烷烃 | B. | 乙烯 | C. | 苯 | D. | 卤代烃 |
5.工业上合成甲醇一般采用下列反应:CO(g)+2H2(g)?CH30H(g)△H,下表是该反应在不同温度下的化学平衡常数(K):
(1)由表中数据判断△H<0(填“>”、“=”或“<”).
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol•L-1,则此时的温度为310℃.
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
①反应从2min到4min之间,H2的反应速率为0.3mol•L-1min-1.
②反应达到平衡时CO的转化率为62.5%.
③反应在第2min时改变了反应条件,改变的条件可能是a(填序号).
a.使用催化剂 b.降低温度 c.增加H2的浓度
(4)常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(l)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1
(5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳.该电池的负极反应式为:CH3OH+H2O=CO2+6H++6e-.若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H2体积(标况)为67.2 L.
| 温度/℃ | 250 | 310 | 350 |
| K/(mol•L-1)-2 | 2.041 | 0.250 | 0.012 |
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol•L-1,则此时的温度为310℃.
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 浓度mol•L-1 时间/min | C(CO) | C(H2) | C(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | x | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
②反应达到平衡时CO的转化率为62.5%.
③反应在第2min时改变了反应条件,改变的条件可能是a(填序号).
a.使用催化剂 b.降低温度 c.增加H2的浓度
(4)常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(l)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1
(5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳.该电池的负极反应式为:CH3OH+H2O=CO2+6H++6e-.若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H2体积(标况)为67.2 L.