题目内容
【题目】图是产生和收集气体的实验装置,该装置适合于( ) 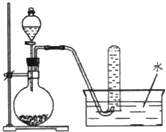
A.用浓硝酸与Cu反应制取NO2
B.用浓盐酸和MnO2反应制取Cl2
C.用H2O2溶液和MnO2反应制取O2
D.用NH4Cl溶液和Ca(OH)2反应制取NH3
【答案】C
【解析】解:A.浓硝酸与铜反应不需加热,但生成的二氧化氮与水反应,故A错误;
B.浓盐酸和二氧化锰反应制取氯气需要加热,且生成的氯气能和水反应,不能用图示装置,故B错误;
C.用H2O2溶液和MnO2反应制取O2,该反应是固体和液体不需加热型,且生成的氧气难溶于水,可用排水法收集,故C正确;
D.氯化铵和氢氧化钙反应是固体和固体反应,制取氨气需要加热,且氨气易溶于水,不能用排水法收集,故D错误.
故选C.
该装置涉及发生装置和收集装置,发生装置适用于固体(或液体)与液体不需加热制气体,收集装置为排水法收集,制取的气体难溶于水,以此解答该题.

练习册系列答案
相关题目