题目内容
13.下列物质能够导电的是( )| A. | 熔融的氢氧化钠 | B. | 硝酸钾溶液 | C. | 硫酸铜晶体 | D. | 无水乙醇 |
分析 能导电的物质中含有自由电子或自由移动的阴阳离子,据此即可解答.
解答 解:A、熔融的氢氧化钠中含有自由移动的阴阳离子,能导电,故A正确;
B、硝酸钾溶液中含有自由移动的阴阳离子,能导电,故B正确;
C、晶体中的离子不能自由移动,不导电,故C错误;
D、无水乙醇中不含有离子,不导电,故D错误.
故选AB.
点评 本题考查了电解质的导电性,注意导电是在水溶液或熔化状态下为条件,题目难度不大.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
4.下列说法正确的是( )
| A. | NH3的摩尔质量为17g | |
| B. | 48gO3含有的臭氧分子数为6.02×1023 | |
| C. | 1mol•L-1NaCl溶液中含1molNa+ | |
| D. | 标准状况下,1molH2O的体积为22.4 L |
1.学习化学可以防止走入生活和学习的误区.你认为下列说法不正确的是( )
| A. | 水银不是银,而是金属汞 | B. | 纯碱不是碱,而是盐 | ||
| C. | 干冰不是冰,而是固体二氧化碳 | D. | 烧碱不是碱,而是一种常见的盐 |
18.下列有关工业生产的叙述正确的是( )
| A. | 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 | |
| B. | 硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 | |
| C. | 炼铁是铁矿石在高温下被氧化的过程 | |
| D. | 钴的制备:3Co3O4+8Al$\stackrel{高温}{→}$9Co+4Al2O3 |
2.按原子序数递增的顺序(稀有气体除外),对第三周期元素性质的描述正确的是( )
| A. | 原子半径和离子半径均减小 | |
| B. | 氧化物对应的水化物碱性减弱,酸性增强 | |
| C. | 非金属气态氢化物稳定性逐渐增强 | |
| D. | 单质的熔点降低 |
3.将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变则下列说法正确的是( )
| A. | 反应过程只有O2生成,共6.72 L的气体(标况) | |
| B. | 本过程一共涉及了三个化学反应 | |
| C. | 最终得到氢氧化铝的沉淀 | |
| D. | 最终得到的溶液中c(NaCl)=0.15 mol•L-1 |

 名称为3-甲基-2-丙基-1-戊烯.
名称为3-甲基-2-丙基-1-戊烯. 名称为1-甲基-3-乙基苯.
名称为1-甲基-3-乙基苯. 名称为:2,4-二甲基-3-乙基戊烷.
名称为:2,4-二甲基-3-乙基戊烷.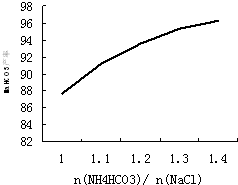 碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:
碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空: