题目内容
【题目】下列气体中既可用浓硫酸干燥,又可用固体氢氧化钠干燥的是( )
A.Cl2B.O2
C.SO2D.NH3
【答案】B
【解析】
A、Cl2与碱反应,所以Cl2不能用固体氢氧化钠干燥,故不选A;
B、O2与浓硫酸、氢氧化钠都不反应,所以O2既可用浓硫酸干燥,又可用固体氢氧化钠干燥,故选B;
C、SO2与碱反应,所以SO2不能用固体氢氧化钠干燥,故不选C;
D、NH3与酸反应,所以NH3不能用浓硫酸干燥,故不选D;
故答案选B。

 53随堂测系列答案
53随堂测系列答案【题目】一定量的铁粉在氯气中充分燃烧,将所得固体完全溶解于稀盐酸,制得溶液A。
(1)铁在氯气中燃烧的化学方程式是___________________________________________。
(2)推测A中可能含有的金属阳离子:①只有Fe3+;②只有Fe2+;③____________________________________。甲同学为探究溶液的组成,实验如下:
实验步骤 | 实验现象 | 实验结论及反应的离子方程式 |
取少量溶液A于试管中,加入KSCN溶液 | ________________ | 假设②不成立,假设①或③成立;反应的离子方程式是________________ |
(3)乙同学继续探究溶液A的组成。
查阅资料:16HCl+2KMnO4===2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:另取少量溶液A于试管中,逐滴加入酸性KMnO4溶液,充分振荡,KMnO4溶液紫色褪去,实验结论:________(填字母序号)。
a.可能有Fe2+ b.可能无Fe2+ c.一定有Fe2+
根据你选择的实验结论,简述理由:_______________________________________________。
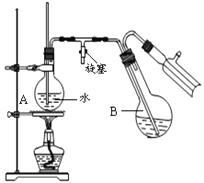
【题目】(1)A、B、C、D为中学常见的混合物分离或提纯的基本装置,请回答:
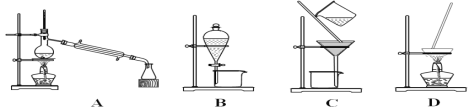
①分离植物油和水,选择装置______(填序号),主要使用仪器名称______;
②分离乙二醇和丙三醇的混合溶液,选择装置______(填序号)。
物质 | 熔点 (摄氏度) | 沸点(摄氏度) | 密度(g/cm-3) | 溶解性 |
乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比例互溶 |
(2)实验室需配制250mL0.1mol·L-1的Na2CO3溶液,填空并回答下列问题:
①配制250mL0.1mol·L-1的Na2CO3溶液,实际应称取Na2CO3的质量是______g,实验过程中所需的玻璃仪器有______。
②若在溶液配制过程中出现如下情况,对所配溶液浓度将有何影响(填“偏高”“偏低”或“无影响”)
若容量瓶中有少量蒸馏水__________;若定容时俯视刻度线__________。
(3)焦炭与浓硫酸加热条件下发生如下反应:C +2H2 SO4(浓)=2SO2↑+ CO2↑ +2H2O,当反应中转移2mole—时,生成SO2的体积(标准状况)是____L。