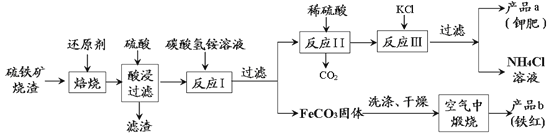
ЬтФПФкШн
ЁОЬтФПЁПЗЯЦјжаЕФ H2S ЭЈЙ§ИпЮТШШЗжНтПЩжЦШЁЧтЦјЃК2H2S(g) ![]() 2H2(g)+S2(g)ЁЃЯждк 3L УмБеШнЦїжаЃЌПижЦВЛЭЌ ЮТЖШНјаа H2S ЗжНтЪЕбщЁЃ
2H2(g)+S2(g)ЁЃЯждк 3L УмБеШнЦїжаЃЌПижЦВЛЭЌ ЮТЖШНјаа H2S ЗжНтЪЕбщЁЃ
(1)ФГЮТЖШЪБЃЌВтЕУЗДгІЬхЯЕжагаЦјЬх 1.31molЃЌЗДгІ tmin КѓЃЌВтЕУЦјЬхЮЊ 1.37molЃЌдђ tmin Фк H2 ЕФЩњГЩ ЫйТЪЮЊ___________________ЁЃ
(2) ФГЮТЖШЪБЃЌПЩзїЮЊХаЖЯЗДгІДяЕНЦНКтЕФБъжОвРОнЪЧ_____ЃЈбЁЬюБрКХЃЉЁЃ
a. ЦјЬхЕФбЙЧПВЛЗЂЩњБфЛЏ b. ЦјЬхЕФУмЖШВЛЗЂЩњБфЛЏ
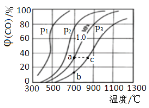
(3)ЪЕбщНсЙћШчЭМЁЃЭМжаЧњЯп a БэЪО H2S ЕФЦНКтзЊЛЏТЪгыЮТЖШЙиЯЕЃЌЧњЯпb БэЪОВЛЭЌЮТЖШЯТЁЂЗДгІОЙ§ЯрЭЌЪБМфЧвЮДДяЕНЛЏбЇЦНКтЪБ H2S ЕФзЊЛЏТЪЁЃ

ИУЗДгІЮЊ________ЗДгІЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЁЃдкШнЦїЬхЛ§ВЛБфЕФЧщПіЯТЃЌ ШчЙћвЊЬсИп H2ЕФЬхЛ§ЗжЪ§ЃЌПЩВЩШЁЕФвЛжжДыЪЉЪЧ_______________________
(4)ЪЙ 1LH2S гы 20L ПеЦјЃЈПеЦјжа O2 ЬхЛ§ЗжЪ§ЮЊ 0.2ЃЉЭъШЋЗДгІКѓЛжИДЕНЪвЮТЃЌЛьКЯЦјЬхЕФЬхЛ§ЪЧ________LЁЃШє 2gH2S ЭъШЋШМЩеКѓЩњГЩЖўбѕЛЏСђКЭЫЎеєЦјЃЌЭЌЪБЗХГі 29.4kJ ЕФШШСПЃЌИУЗДгІЕФШШЛЏбЇЗНГЬЪНЪЧ_________________ЁЃ
ЁОД№АИЁП0.04/t mol/(LЁЄmin) a ЮќШШ Щ§ИпЗДгІЮТЖШЃЌМАЪБЗжРыS2ЦјЬхЕШЃЈШЮаДвЛЬѕЃЌКЯРэМДПЩЃЉ 19.5 2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ![]() H =-999.6KJ/mol
H =-999.6KJ/mol
ЁОНтЮіЁП
ДЫЬтЪЧвЛЛЏбЇЦНКтзлКЯЬтЃЌЩцМАЛЏбЇЦНКтЛљБОМЦЫуЃЌЛљБОХаЖЯжЊЪЖБШНЯЛљДЁЁЃ
ЃЈ1ЃЉИљОнЗНГЬЪНПЩжЊУПЩњГЩ2molЧтЦјЃЌЦјЬхМѕЩй1LЁЃФГЮТЖШЪБЃЌВтЕУЗДгІЬхЯЕжагаЦјЬх1.31molЃЌЗДгІ1 minКѓЃЌВтЕУЦјЬхЮЊ1.37molЃЌЦјЬхМѕЩй0.06molЃЌЫљвдЩњГЩЧтЦјЪЧ0.12molЃЌХЈЖШЪЧ0.04mol/LЃЌдђtmin ФкH2ЕФЩњГЩЫйТЪЮЊ0.04/t mol/(LЁЄmin)ЁЃ
ЃЈ2ЃЉaЃЎе§ЗДгІЬхЛ§діМгЃЌдђЦјЬхЕФбЙЧПВЛЗЂЩњБфЛЏЫЕУїДяЕНЦНКтзДЬЌЃЌЙЪaе§ШЗЃЛ
bЃЎУмЖШЪЧЛьКЯЦјЬхЕФжЪСПКЭШнЦїШнЛ§ЕФБШжЕЃЌжЪСПКЭШнЛ§ОљВЛБфЃЌвђДЫЦјЬхЕФУмЖШВЛЗЂЩњБфЛЏВЛФмЫЕУїДяЕНЦНКтзДЬЌЃЌbДэЮѓЃЛ
ЃЈ3ЃЉИљОнЭМЯёПЩжЊЩ§ИпЮТЖШзЊЛЏТЪдіДѓЃЌЫЕУїЩ§ИпЮТЖШЦНКтЯђе§ЗДгІЗНЯђНјааЃЌвђДЫИУЗДгІЮЊЮќШШЗДгІЁЃе§ЗДгІЪЧЬхЛ§діДѓЁЂЮќШШЕФПЩФцЗДгІЃЌвђДЫдкШнЦїЬхЛ§ВЛБфЕФЧщПіЯТЃЌШчЙћвЊЬсИпH2ЕФЬхЛ§ЗжЪ§ЃЌПЩВЩШЁЕФДыЪЉЪЧЩ§ИпЗДгІЮТЖШЃЌМАЪБЗжРыS2ЦјЬхЕШЁЃ
ЃЈ4) 20LПеЦјжабѕЦјЕФЬхЛ§ЪЧ20LЁС0.2=4LЃЌбѕЦјКЭH2SЗДгІЕФЗНГЬЪНЮЊ2H2S+3O2=2SO2+2H2OЃЌетЫЕУїбѕЦјЙ§СПЃЌЪЃгрбѕЦјЪЧ4LЃ1.5LЃН2.5LЃЛЩњГЩSO2ЪЧ1LЃЌдђЭъШЋЗДгІКѓЛжИДЕНЪвЮТЃЌЛьКЯЦјЬхЕФЬхЛ§ЪЧ16LЃЋ2.5LЃЋ1LЃН19.5LЁЃШє2gH2SЭъШЋШМЩеКѓЩњГЩЖўбѕЛЏСђКЭЫЎеєЦјЃЌЭЌЪБЗХГі29.4 kJЕФШШСПЃЌдђ2molH2SЭъШЋЗДгІЗХГіЕФШШСПЪЧ999.6KJЃЌвђДЫИУЗДгІЕФШШЛЏбЇЗНГЬЪНЪЧ 2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ![]() H=-999.6kJ/mol
H=-999.6kJ/mol

ЁОЬтФПЁПНЋH2SзЊЛЏЮЊПЩдйРћгУЕФзЪдДЪЧФмдДбаОПСьгђЕФживЊПЮЬтЁЃ
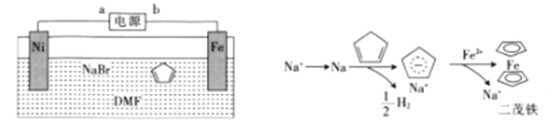
ЃЈ1ЃЉH2SЕФзЊЛЏ
Ђё | ПЫРЭЫЙЗЈ |
|
Ђђ | ЬњбЮбѕЛЏЗЈ |
|
Ђѓ | ЙтЗжНтЗЈ |
|
Ђй ЗДгІЂёЕФЛЏбЇЗНГЬЪНЪЧ________ЁЃ
Ђк ЗДгІЂђЃК____+ 1 H2S ==____Fe2+ + ____SЁ§ + ____ЃЈНЋЗДгІВЙГфЭъећЃЉЁЃ
Ђл ЗДгІЂѓЬхЯжСЫH2SЕФЮШЖЈадШѕгкH2OЁЃНсКЯдзгНсЙЙНтЪЭЖўепЮШЖЈадВювьЕФдвђЃК_______ЁЃ
ЃЈ2ЃЉЗДгІЂѓСђЕФВњТЪЕЭЃЌЗДгІЂђЕФдзгРћгУТЪЕЭЁЃЮвЙњПЦбаШЫдБЩшЯыНЋСНИіЗДгІёюКЯЃЌЪЕЯжгЩH2SИпаЇВњЩњSКЭH2ЃЌЕчзгзЊвЦЙ§ГЬШчЭМЁЃ
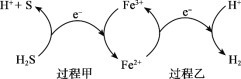
Й§ГЬМзЁЂввжаЃЌбѕЛЏМСЗжБ№ЪЧ______ЁЃ
ЃЈ3ЃЉАДееЩшМЦЃЌПЦбаШЫдБбаОПШчЯТЁЃ
Ђй ЪзЯШбаОПЙ§ГЬввЪЧЗёПЩааЃЌзАжУШчЭМЁЃОМьбщЃЌnМЋЧјВњЩњСЫFe3+ЃЌpМЋВњЩњСЫH2ЁЃnМЋЧјВњЩњFe3+ЕФПЩФмдвђЃК
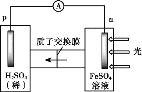
ЂЁЃЎFe2+ - e- = Fe3+
ЂЂЃЎ2H2O -4e-=O2 +4H+ЃЌ_______ЃЈаДРызгЗНГЬЪНЃЉЁЃОШЗШЯЃЌЂЁЪЧВњЩњFe3+ЕФдвђЁЃЙ§ГЬввПЩааЁЃ
Ђк ЙтееВњЩњFe3+КѓЃЌЯђnМЋЧјзЂШыH2SШмвКЃЌгаSЩњГЩЃЌГжајВњЩњЕчСїЃЌpМЋВњЩњH2ЁЃбаОПSВњЩњЕФдвђЃЌЩшМЦШчЯТЪЕбщЗНАИЃК______ЁЃ ОШЗШЯЃЌSЪЧгЩFe3+бѕЛЏH2SЫљЕУЃЌH2SВЛФмжБНгЗХЕчЁЃЙ§ГЬМзПЩааЁЃ
ЃЈ4ЃЉзлЩЯЃЌЗДгІЂђЁЂЂѓФмёюКЯЃЌЭЌЪБФмИпаЇВњЩњH2КЭSЃЌЦфЙЄзїдРэШчЭМЁЃ
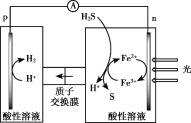
НјвЛВНбаОПЗЂЯжЃЌГ§СЫFe3+/Fe2+ ЭтЃЌI3-/I- вВФмЪЕЯжШчЭМЫљЪОбЛЗЙ§ГЬЁЃНсКЯЛЏбЇгУгяЃЌЫЕУїI3-/I- ФмЙЛЪЙSдДдДВЛЖЯВњЩњЕФдвђЃК________ЁЃ
ЁОЬтФПЁПвдЙшдхЭСЮЊдиЬхЕФЮхбѕЛЏЖўЗАЃЈV2O5ЃЉЪЧНгДЅЗЈЩњГЩСђЫсЕФДпЛЏМСЁЃДгЗЯЗАДпЛЏМСжаЛиЪеV2O5МШБмУтЮлШОЛЗОГгжгаРћгкзЪдДзлКЯРћгУЁЃЗЯЗАДпЛЏМСЕФжївЊГЩЗжЮЊЃК
ЮяжЪ | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
жЪСПЗжЪ§/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | ЃМ1 |
вдЯТЪЧвЛжжЗЯЗАДпЛЏМСЛиЪеЙЄвеТЗЯпЃК

ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЁАЫсНўЁБЪБV2O5зЊЛЏЮЊVO2+ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ___________ЃЌЭЌЪБV2O4зЊГЩVO2+ЁЃЁАЗЯдќ1ЁБЕФжївЊГЩЗжЪЧ__________________ЁЃ
ЃЈ2ЃЉЁАбѕЛЏЁБжагћЪЙ3 molЕФVO2+БфЮЊVO2+ЃЌдђашвЊбѕЛЏМСKClO3жСЩйЮЊ______molЁЃ
ЃЈ3ЃЉЁАжаКЭЁБзїгУжЎвЛЪЧЪЙЗАвдV4O124аЮЪНДцдкгкШмвКжаЁЃЁАЗЯдќ2ЁБжаКЌга_______ЁЃ
ЃЈ4ЃЉЁАРызгНЛЛЛЁБКЭЁАЯДЭбЁБПЩМђЕЅБэЪОЮЊЃК4ROH+ V4O124![]() R4V4O12+4OHЃЈвдROHЮЊЧПМюадвѕРызгНЛЛЛЪїжЌЃЉЁЃЮЊСЫЬсИпЯДЭбаЇТЪЃЌСмЯДвКгІИУГЪ_____адЃЈЬюЁАЫсЁБЁАМюЁБЁАжаЁБЃЉЁЃ
R4V4O12+4OHЃЈвдROHЮЊЧПМюадвѕРызгНЛЛЛЪїжЌЃЉЁЃЮЊСЫЬсИпЯДЭбаЇТЪЃЌСмЯДвКгІИУГЪ_____адЃЈЬюЁАЫсЁБЁАМюЁБЁАжаЁБЃЉЁЃ
ЃЈ5ЃЉЁАСїГівКЁБжабєРызгзюЖрЕФЪЧ________ЁЃ
ЃЈ6ЃЉЁАГСЗАЁБЕУЕНЦЋЗАЫсяЇЃЈNH4VO3ЃЉГСЕэЃЌаДГіЁАьбЩеЁБжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН____________ЁЃ