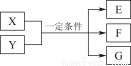
题目内容
银氨溶液放久后会产生叠氮化银(AgN3)而引起爆炸,直接排放会污染环境,且造成银资源的浪费。某研究小组设计了从银镜反应后的废液中(含过量的银氨溶液,假设不含单质银)回收银的如下两种实验流程:
(已知:[Ag(NH3)2]+在溶液中存在平衡:[Ag(NH3)2]+??Ag++2NH3)
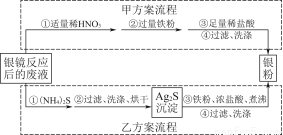
(1)写出甲方案第①步废液与稀HNO3反应的离子方程式 。
(2)甲方案第②步加入的铁粉要过量的目的是 。
甲方案流程可能产生的大气污染物是 。
(3)乙方案若最终得到银粉的质量偏大,排除未洗涤干净的因素,可能的原因是 。
(4)实验室配制银氨溶液的操作过程是 。
(5)已知乙方案第③步反应有H2S气体产生,若最终得到银粉21.6 g,不考虑其他损失,理论上该步需要加入铁粉 g。
(1)Ag[(NH3)2]++OH-+3H+=Ag++2NH4++H2O
(2)使溶液中的Ag+全部被还原 NO
(3)铁粉或Ag2S未反应完混于其中
(4)在洗净的试管中,注入1 mL AgNO3溶液,然后逐滴加入氨水,边滴边振荡,直到最初生成的沉淀刚好溶解为止(没有强调“洗净”不算全对,氨水与AgNO3具体浓度不作要求)
(5)5.6
【解析】甲方案可解读为:向银氨溶液中加入稀硝酸,使平衡([Ag(NH3)2]+??Ag++2NH3)右移,破坏银氨溶液,再加入过量铁粉置换Ag+,最后加入过量稀盐酸溶解过量的铁粉,过滤、洗涤得银粉。但此方案中过量的稀硝酸可能与铁反应生成污染性气体NO。乙方案可解读为:向银氨溶液中加入(NH4)2S使Ag+转化为Ag2S沉淀,获取Ag2S后与浓盐酸、铁粉加热煮沸使发生反应:Ag2S+2HCl+Fe=2Ag+FeCl2+H2S,由方程式看出,要获得0.2 mol Ag,需要加入0.1 mol Fe。

 阅读快车系列答案
阅读快车系列答案为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验Ⅰ 反应产物的定性探究
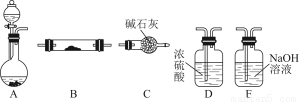
实验装置如图所示。(固定装置已略去)
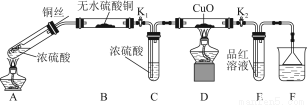
(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是 。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
实验Ⅱ 反应产物的定量探究
(6)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1:
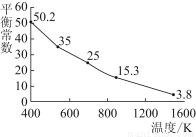
硫酸/mol·L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
15 | 约150 | 约236 |
16 | 约140 | 约250 |
18 | 约120 | 不消失 |
资料2:X射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。仅由上述资料可得出的正确结论是 __。
a.铜与浓硫酸反应时所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免最后产物中出现黑色物质
c.该反应发生的条件之一是硫酸浓度≥15 mol·L-1
d.硫酸浓度越大,黑色物质越快出现、越难消失
(7)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol·L-1Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为 _。(已知:2Cu2++4I-=2CuI+I2,2S2O32-+I2=S4O62-+2I-)