题目内容
【题目】如图是某同学研究铜与浓硫酸的反应装置:
完成下列填空:
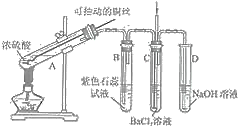
(1)写出A中发生反应的化学方程式______,采用可抽动铜丝进行实验的优点是______。
(2)反应一段时间后,可观察到B试管中的现象为______。
(3)从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是______、______.(要求填一种化合物和一种单质的化学式)。
(4)反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是______,该黑色不溶物不可能是CuO,理由是______。
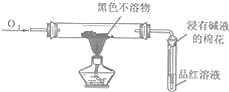
(5)对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:
实验装置 | 实验现象 |
| 品红褪色 |
①根据实验现象可判断黑色不溶物中一定含有______元素。
②若该黑色不溶物由两种元素组成且在反应前后质量保持不变,推测其化学式为______。
【答案】Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑ 可以控制反应的进行 变红 NH3 Cl2 过滤 CuO会溶于稀硫酸中 硫 Cu2S
CuSO4+2H2O+SO2↑ 可以控制反应的进行 变红 NH3 Cl2 过滤 CuO会溶于稀硫酸中 硫 Cu2S
【解析】
(1)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,由此可写出化学方程式;
(2)反应生成二氧化硫,能够与水反应生成亚硫酸,遇到石蕊显红色;
(3)向BaCl2溶液中通入另一种气体,产生白色沉淀,是因为二氧化硫不与氯化钡溶液反应,通入的气体需要满足把二氧化硫转化为盐或把二氧化硫氧化为硫酸;
(4)分离固体与液体可以采用过滤法,氧化铜与酸反应生成铜离子与水;
(5)黑色固体通入氧气反应生成气体能够使品红褪色,说明生成二氧化硫,含有硫元素;若该黑色不溶物由两种元素组成且在反应前后质量保持不变,可知除了含有硫元素外还含有铜。
(1)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑,抽动铜丝可以控制铜丝与浓硫酸接触面积从而控制反应进行,故答案为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,抽动铜丝可以控制铜丝与浓硫酸接触面积从而控制反应进行,故答案为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;可以控制反应的进行;
CuSO4+2H2O+SO2↑;可以控制反应的进行;
(2)反应生成二氧化硫,二氧化硫为酸性氧化物,能够与水反应生成亚硫酸,溶液显酸性,遇到石蕊显红色,故答案为:变红;
(3)向BaCl2溶液中通入另一种气体,产生白色沉淀,是因为二氧化硫不与氯化钡溶液反应,通入的气体需要满足把二氧化硫转化为盐或把二氧化硫氧化为硫酸,如碱性气体NH3、做氧化剂的气体如Cl2、O2、O3、NO2、Cl2O等,故答案为:NH3;Cl2 ;
(4)将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离固体与液体可以采用过滤法;氧化铜与酸反应生成铜离子与水,所以黑色固体不可能为氧化铜,故答案为:过滤;CuO会溶于稀硫酸中;
(5)黑色固体通入氧气反应生成气体能够使品红褪色,说明生成二氧化硫,含有硫元素;若该黑色不溶物由两种元素组成且在反应前后质量保持不变,可知除了含有硫元素外还含有铜,物质为硫化亚铜,化学式为Cu2S,故答案为:硫;Cu2S。

【题目】用如图装置进行实验;下列预期实验现象及相应结论均正确的是( )

a | b | 预期实验现象 | 结论 | |
A | 铜丝 | 浓硝酸 | 试管c中有大量红棕色气体 | 硝酸有强氧化性 |
B | 木条 | 18.4mol/L硫酸 | 木条变黑 | 浓硫酸有酸性及氧化性 |
C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 |
D | 铁丝 | 含少量HCl的H2O2溶液 | 试管c中有大量无色气体 | 该反应中铁作催化剂 |
A. A B. B C. C D. D