��Ŀ����
����Ŀ��Ǧ���������ұ������Ǧ������Ҫ�ɷ�ΪPbS��
I.����Ǧ��Ǧ�����ڿ����б��գ�����PbO��SO2��
����Ǧ�������Ǧ�ķ�Ӧ�Ļ�ѧ����ʽΪ___��
�ڻ���Ǧ�ķ����к���Ũ��SO2���ɽ�����ͨ�������ˮ�н��д�������Ӧ�����ӷ���ʽΪ___��
II.ʪ����Ǧ���Ʊ�����Ǧ��ͬʱ�������Ƶ���ǣ�����ڻ���Ǧ��Ϊ������ʪ����Ǧ�Ĺ���������ͼ��

��֪���ٲ�ͬ�¶���PbCl2���ܽ�����±���ʾ��

��PbCl2Ϊ������ˮ��������ʣ���Cl-Ũ�Ƚϴ����Һ�У�����ƽ�⣺PbCl2(aq)+2Cl-(aq)![]() PbCl42-(aq)��
PbCl42-(aq)��
��3��Ǧ�����ȡ�������ȹ�������ԭ����___��
��4������aΪ������ˮϡ�Ͳ���ȴ���ò�����������Һ1��PbCl2���������Է�����������ˮϡ�������ܵ�ԭ����___��
��5������Һ3����Һ2�ֱ�������ͼ��ʾ���װ�õ����������У�����ȡ����Ǧ��ʹ��ȡҺ�е�FeCl3������

����Һ3Ӧ����___(������������������������)�С�
����Һ2�����ʵ��FeCl3���������õ缫�ĵ缫��Ӧʽ___��
����Ǧ���������Ϊag��Ǧ������Ϊb����������ͨ��cmol����ʱ������Ǧȫ��������Ǧ������PbS����������Ϊ___����a��b��c�Ĵ���ʽ��ʾ����
���𰸡�2PbS+3O2![]() 2PbO+SO2 2NH3H2O+SO2=2NH4++SO32-+H2O ��ֹ�¶Ƚ��ͣ�PbCl2�ܽ�Ƚ��Ͷ�������� ������ˮϡ�ͣ�ʹPbCl2+2Cl-PbCl42-ƽ�������ƶ� ������ Fe2+-e=Fe3+
2PbO+SO2 2NH3H2O+SO2=2NH4++SO32-+H2O ��ֹ�¶Ƚ��ͣ�PbCl2�ܽ�Ƚ��Ͷ�������� ������ˮϡ�ͣ�ʹPbCl2+2Cl-PbCl42-ƽ�������ƶ� ������ Fe2+-e=Fe3+ ![]()
��������
II.Ǧ����ͨ�������Ȼ������Ȼ�����Һ���ݣ����ȣ����ȹ��ˣ��õ����Ȼ�Ǧ���Ȼ���������Һ�ͺ������ʵ���������Һ������ˮϡ�Ͳ���ȴ���õ��Ȼ�������Һ������PbCl2��PbCl2�����Ȼ�����Һ��ʹƽ��PbCl2(aq)+2Cl-(aq)PbCl42-(aq)�����ƶ����õ�PbCl42-��Һ�������������Ȼ�������Һ��ͬ��ɵ��أ����õ�Ǧ���ʺͺ����Ȼ�������Һ��
(1)�������֪��Ǧ�����ڿ����б��գ�PbS��������Ӧ����PbO��SO2����Ӧ�Ļ�ѧ����ʽΪ2PbS+3O2![]() 2PbO+SO2��
2PbO+SO2��
(2)���������������������ˮ�������ԣ���ˮ���������Ӧ����������狀�ˮ����Ӧ�����ӷ���ʽΪ��2NH3H2O+SO2�T2NH4++SO32-+H2O��
(3)������Ŀ��Ϣ��֪PbCl2���¶ȵ�ʱ�ܽ�Ƚ�С�����ȹ��˿ɷ�ֹPbCl2���������ģ�
(4)PbCl2Ϊ������ˮ��������ʣ�����ƽ�⣺PbCl2(aq)+2Cl-(aq)PbCl42-(aq)����ˮϡ�ͣ�ƽ�������ƶ�����ȴ���¶Ƚ��ͣ�PbCl2���ܽ�Ƚ��ͣ��Ӷ�����PbCl2���壻
(5)����Һ3�Ǻ�PbCl42-����Һ��Ҫ�Ƶõ���Ǧ��Ԫ��Ǧ�Ļ��ϼ۽��ͣ��õ����ӣ�������ԭ��Ӧ�����ݵ��صĹ���ԭ���������õ����ӣ�����Һ3Ӧ���������ң�
������������Һ2����Һ2���Ȼ�������Һ����������������ʧȥ���ӣ�ת�������������ӣ���Һ�е�������������ͨ�������ӽ���Ĥ�����������ң������������ӽ�ϣ��õ��Ȼ�����Һ���ﵽ������Ŀ�ģ��������������缫��Ӧ��Fe2+-e-�TFe3+��
�۵�������Pb2+��Pb��1molPb2+ת��2mol���ӣ���������ͨ��c mol����ʱ������Ǧȫ�����������Ծ���![]() c mol��Pb������Ǧ������Ϊb����ԭҺ����Ǧ�������ʵ���Ϊ
c mol��Pb������Ǧ������Ϊb����ԭҺ����Ǧ�������ʵ���Ϊ![]() mol����PbS�����ʵ���ҲΪ
mol����PbS�����ʵ���ҲΪ![]() mol��m(PbS)=(207+32)g/mol��
mol��m(PbS)=(207+32)g/mol��![]() mol=
mol=![]() g��Ǧ���������Ϊa g����������=
g��Ǧ���������Ϊa g����������=![]() ��
��

 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�����Ŀ�������йط�Ӧ�ȵ���������ȷ���� (����)
����֪2H2(g)+O2(g)=2H2O(g)����H=-483.6 kJ�� mol-1����������ȼ������H=-241.8 kJ�� mol-1
���ɵ���Aת��Ϊ����B��һ�����ȹ��̣��ɴ˿�֪����B�ȵ���A�ȶ�
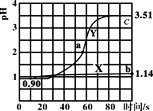
��X(g)+Y(g)![]() Z(g)+W(s)����H>0�����º��������´ﵽƽ������X��������Ӧ����H����
Z(g)+W(s)����H>0�����º��������´ﵽƽ������X��������Ӧ����H����
����֪���±����ݿ��Լ����![]() (g)+3H2(g)
(g)+3H2(g)![]()
![]() (g)���ʱ�
(g)���ʱ�
���ۼ� | C��C | C=C | C��H | H��H |
����/(kJ��mol-1) | 348 | 610 | 413 | 436 |
�ݸ��ݸ�˹���ɿ���֪����ͬ�����£����ʯ��ʯīȼ������1 mol CO2(g)ʱ���ų����������
��25 ����101 kPaʱ��1 mol̼��ȫȼ������CO2(g)���ų�������Ϊ̼��ȼ����
A.�٢ڢۢ�B.�ۢܢ�C.�ܢ�D.��