题目内容
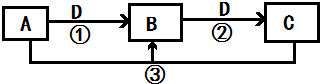
8.物质M是一种日常生活中不可缺少的调味品.已知C在D中燃烧发生苍白色火焰,M与其他物质的转化关系如图甲所示(部分产物已略去);
(1)写出用惰性电极电解M溶液的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)比较B中各元素原子半径大小Na>O>H(填元素符号).
(3)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是H2SiO3.
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是溶液中逐渐有白色絮状沉淀生成,且不断增加,然后又由多到少,最后消失.
(5)若A是一种溶液,只可能含有H+,NH4+,Mg2+,Fe3+,Al3+,CO32-,SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图乙所示.由此可知,该溶液中肯定含有的离子及其浓度之比为c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3.
(6)若E可用于检验葡萄糖的存在,写出G溶液充分蒸发灼烧后的产物与乙醇反应的化学方程式2CH3CH2OH+CuO$\stackrel{△}{→}$2CH3CHO+Cu+2H2O.
(7)根据下图,写出25℃时由CO2和H2O转化为葡萄糖溶液的化学方程式6CO2(g)+6H2O(l)$\stackrel{△}{→}$C6H12O6(aq)+2H2O(g).

分析 (1)C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H2、D为Cl2、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解生成氢气、氯气与B,可推知M为NaCl、B为NaOH,
(2)B为NaOH,根据原子电子层数越多半径越大,电子层数相同时则核电荷数越多,半径越小,据此判断;
(3)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2,E为Na2SiO3,与F溶液反应得到G为H2SiO3;
(4)若A是一种常见金属单质,且与NaOH溶液能够反应,则A为Al,E为NaAlO2,则将过量的HCl溶液逐滴加入NaAlO2溶液中,先生成氢氧化铝,而后氢氧化铝溶解;
(5)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO32-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则含有NH4+,由电荷守恒可知一定含有SO42-,根据各阶段消耗的NaOH体积结合离子方程式计算n(H+):n(Al3+):n(NH4+)之比,再结合电荷守恒计算与n(SO42-)的比例关系,据此计算;
若A是一种盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,可推知A中含有Fe2+,E为Fe(OH)3,G为FeCl3;
(6)若E可用于检验葡萄糖的存在,则E为氢氧化铜,E和F生成G,则G为氯化铜,由于铜离子能水解,氯化把易挥发,所以氯化铜溶液充分蒸发灼烧后的产物为氧化铜,氧化铜与乙醇发生氧化还原反应生成铜和乙醛,据此答题;
(7)根据图中各物质转化关系及元素守恒可写出由CO2和H2O转化为葡萄糖溶液的化学方程式.
解答 解:(1)C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H2、D为Cl2、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解生成氢气、氯气与B,可推知M为NaCl、B为NaOH,用惰性电极电解M溶液的离子方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑,
故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;
(2)B为NaOH,根据原子电子层数越多半径越大,电子层数相同时则核电荷数越多,半径越小,所以NaOH中各元素原子半径大小为Na>O>H,
故答案为:Na>O>H;
(3)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2,E为Na2SiO3,与F溶液反应可以得到G为H2SiO3,
故答案为:H2SiO3;
(4)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO32-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则含有NH4+,由电荷守恒可知一定含有SO42-,
发生反应H++OH-=H2O,氢离子消耗NaOH溶液的体积为1积,
发生反应Al3++3OH-=Al(OH)3↓,铝离子消耗NaOH溶液的体积为3体积,
发生反应NH4++OH-=NH3•H2O,铵根消耗氢氧化钠为2体积,
则n(H+):n(Al3+):n(NH4+)=1:1:2,由电荷守恒可知,n(H+):n(Al3+):n(NH4+):n(SO42-)=1:1:2:3,故c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3,
故答案为:c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3;
(6)若E可用于检验葡萄糖的存在,则E为氢氧化铜,E和F生成G,则G为氯化铜,由于铜离子能水解,氯化把易挥发,所以氯化铜溶液充分蒸发灼烧后的产物为氧化铜,氧化铜与乙醇发生氧化还原反应生成铜和乙醛,反应方程式为2CH3CH2OH+CuO$\stackrel{△}{→}$2CH3CHO+Cu+2H2O,
故答案为:2CH3CH2OH+CuO$\stackrel{△}{→}$2CH3CHO+Cu+2H2O;
(7)根据图中各物质转化关系及元素守恒可写出由CO2和H2O转化为葡萄糖溶液的化学方程式为6CO2(g)+6H2O(l)$\stackrel{△}{→}$ C6H12O6(aq)+2H2O(g),
故答案为:6CO2(g)+6H2O(l)$\stackrel{△}{→}$ C6H12O6(aq)+2H2O(g).
点评 本题考查无机物推断等,题目涉及元素化合物较多,需要学生全面掌握据基础知识,注意离子方程式与电荷守恒的应用,难度中等.

①热稳定性:H2O>HF>H2S
②密度:K<Na<Rb
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④HCl的形成过程:

⑤元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑥结合质子的能力:S2->Cl-
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
| A. | ①②④⑤ | B. | ③⑤⑥⑦ | C. | ②④⑤⑥ | D. | ①③④⑦ |
①Na2CO3-制玻璃;②HNO3-制造氮肥③MgO-耐高温材料;④Na-制过氧化钠;⑤Al2O3-焊接钢轨.
| A. | ①②③ | B. | ②③⑤ | C. | ①②③④ | D. | ①②③④⑤ |
| A. | 黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成 | |
| B. | 可用蘸浓硫酸的棉棒检验输送氨气的管道是否漏气 | |
| C. | 碘是人体必需微量元素,所以要适量吃富含碘酸根原子团的食物 | |
| D. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3;
(3)丙同学设计如下实验方案对甲、乙同学的解释进行判断:
将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此可以判断乙(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中有新物质生成.
| t/s | 0 | 500 | 1000 | 1500 |
| n(N2O5)/mol | 5.00 | 3.5 | 2.50 | 2.50 |
| A. | 500s内N2O5分解速率为3×10-4mol•L-1•s-1 | |
| B. | 反应达平衡后,往容器中加入5molN2O5气体,平衡正向移动,反应的热效应不变 | |
| C. | 相同温度下,将体积缩小为原来的$\frac{1}{2}$,达到新平衡时,N2O5(g)的浓度为0.125mol/L | |
| D. | 达到新平衡的压强是初始时的1.75倍 |
CH4(g)+$\frac{1}{2}$O2(g)?CO(g)+2H2(g)△H<0 ①
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0 ①
下列说法不正确的是( )
| A. | 当反应①中v正(CH4)=v逆(CO)时,表明该反应达平衡状态 | |
| B. | 其他条件不变时,增大体系压强,反应①、②中甲烷的转化率均减小 | |
| C. | 使用高效催化剂可以加快反应速率,同时提高CH4的转化率 | |
| D. | 同一容器内同时发生反应①与②时,容器内温度可能保持不变 |
| A. | 金属铁与硫酸铜溶液反应:2Fe+3Cu2+═2Fe3++3Cu | |
| B. | 碳酸氢钠溶液与氢氧化钠溶液反应:OH-+HCO3-═H2O+CO2↑ | |
| C. | 氢氧化钡溶液与硫酸溶液反应:Ba2++2OH-+2H++SO42-═2H2O+BaSO4↓ | |
| D. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ |