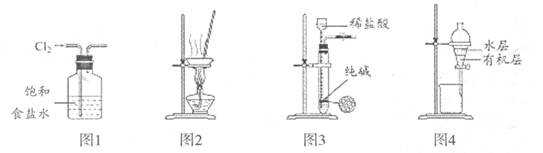
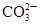题目内容
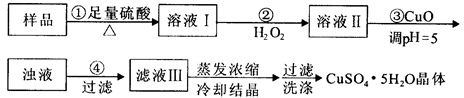
空气吹出法工艺是目前“海水提溴”的最主要方法之一,其工艺流程如下:
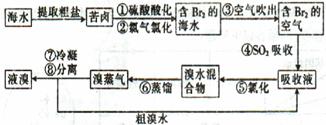
(1)目前,从海水中提取的溴约占世界溴年产量的 。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,其原因是 。
(3)步骤④的离子方程式。
(4)步骤⑥的蒸馏过程中,溴出口温度要控制在80?90℃。温度过高或过低都不利于生产,理由是 。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离。分离仪器的名称是 ,分离吋液溴从分离器的 (填“上口”或“下口”)排出。
(6)不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”的原因是 。
(7)某同学测得苦卤中溴的含量为0.8g·L-1,已知步骤①?⑥中溴共损失了25%,步骤⑦和步骤⑧又共损失了所得溴蒸气的10%,若处理10 m3这样的苦卤,可得到液溴 mol。

(1)目前,从海水中提取的溴约占世界溴年产量的 。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,其原因是 。
(3)步骤④的离子方程式。
(4)步骤⑥的蒸馏过程中,溴出口温度要控制在80?90℃。温度过高或过低都不利于生产,理由是 。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离。分离仪器的名称是 ,分离吋液溴从分离器的 (填“上口”或“下口”)排出。
(6)不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”的原因是 。
(7)某同学测得苦卤中溴的含量为0.8g·L-1,已知步骤①?⑥中溴共损失了25%,步骤⑦和步骤⑧又共损失了所得溴蒸气的10%,若处理10 m3这样的苦卤,可得到液溴 mol。
(1)

(2)酸化可抑制Cl2、Br2与水反应
(3)Br2+SO2+2H2O==4H++2Br-+SO42-
(4)温度过高,大量水蒸气随水排出去,溴蒸气中水分增加,温度过低,溴不能完全蒸出,吸收率低。
(5)分液漏斗;下口
(6)氯化后的海水虽然含有溴单质,但浓度低,如果直接蒸馏原料,产品成本高,“空气吹出、SO2吸收、氯化”的过程实际是一个溴的浓缩过程。
(7)33.75
试题分析:(1)从海水中提取的溴约占世界溴年产量的
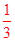 。
。(2)Cl2、Br2与水反应生成酸,加入硫酸可抑制Cl2、Br2与水反应。
(3)步骤④是溴单质将SO2氧化。
(4)温度过高,会增加水蒸气,温度过低,则溴不能完全蒸出。
(5)分离溴水和液溴,应用分液漏斗。因液溴密度大于水,因此液溴从分液漏斗下口排出。
(6)氯化后的海水含溴量低。
(7)
 。
。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目