题目内容
下列有关实验的结论正确的是
| 选项 | 实验操作及现象 | 实验结论 |
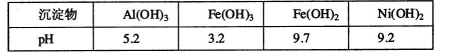
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 溶液中一定含有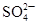 |
| B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色气体 | 溶液中一定含有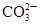 |
| C | 用酸度计测定SO2和CO2饱和溶液的pH,前者pH小 | H2SO3酸性强于H2CO3 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色 | 浓氨水呈碱性 |
D
试题分析:A、可能有银离子干扰,会产生不溶于酸的氯化银沉淀,错误;B、产生能使澄清石灰水变浑浊的无色气体可能是CO32-、HCO3-、SO32-、HSO3-,错误;C、SO2和CO2饱和溶液的浓度不同,前者浓度大,故溶液pH的大小不能判断酸性的强弱,错误;D、正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

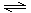 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层) 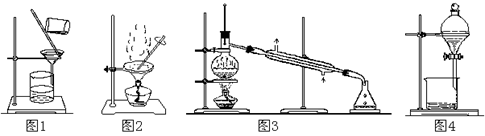
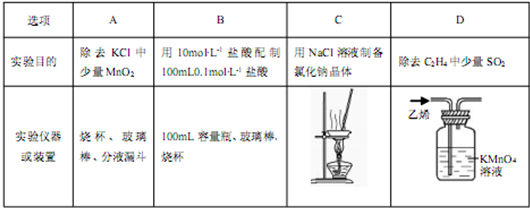
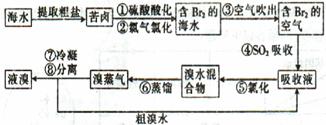
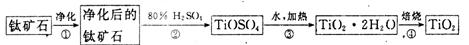
 TiCl4(1)+O2(g) △H=+151 kJ/mol。所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4,请说明判断该反应难以发生的理由是_______。当往氯化反应体系中加入碳后,反应在高温条件下能顺利进行生成TiCl4。
TiCl4(1)+O2(g) △H=+151 kJ/mol。所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4,请说明判断该反应难以发生的理由是_______。当往氯化反应体系中加入碳后,反应在高温条件下能顺利进行生成TiCl4。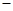 394 kJ/mol。
394 kJ/mol。
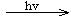 TiO2/S*(激发态)
TiO2/S*(激发态) TiO2/S+ + e-
TiO2/S+ + e-