题目内容
【题目】通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+H2O2+BaCl2=BaSO4↓+2HCl,用NA表示阿伏伽德罗常数的值,下列说法不正确的是
A. 0.1 mol BaCl2中所含离子总数为0.3 NA
B. 25℃时,0.1mol/L的HCl溶液中含有H+的数目为0.1 NA
C. 标准状况下,17 g H2O2中所含分子总数为0.5 NA
D. 生成2.33 g BaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224 L
【答案】B
【解析】A.BaCl2为强电解质,1 mol BaCl2溶液中含有离子总数为3NA;B.溶液的体积未知,无法求出H+的数目;C.根据n=m/M进行计算;D.根据V=m×Vm/M进行计算。
0.1 molBaCl2中含有0.1mol Ba2+和0.2molCl-,所含离子总数约为0.3NA,A正确;没有给定溶液的体积,无法求出0.1mol/L的HCl溶液中含有H+的数目,B错误;17gH2O2的物质的量为![]() =0.5mol,所含分子的物质的量为0.5NA,C正确;2.33gBaSO4的物质的量为
=0.5mol,所含分子的物质的量为0.5NA,C正确;2.33gBaSO4的物质的量为![]() =0.01mol,根据方程式可知,吸收SO20.01mol,在标准状况下的体积为0.01mol×22.4L/mol =0.224L,D正确;答案选B。
=0.01mol,根据方程式可知,吸收SO20.01mol,在标准状况下的体积为0.01mol×22.4L/mol =0.224L,D正确;答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】针对下面10种元素,完成以下各小题.
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是(填名称).
(2)最高价氧化物对应的水化物碱性最强的是(填化学式).
(3)Al的原子结构示意图为 .
(4)S和Cl相比,元素非金属性较强的是 .
(5)可用来制造光导纤维的物质是 , 晶体硅的主要用途是(写出一种).
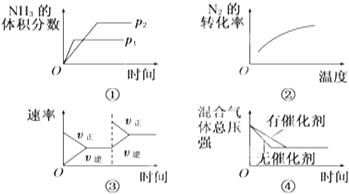
(6)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3 , 请写出反应的化学方程式: .