��Ŀ����
4��������������Դ�������ȷ������Ź㷺����;����ҵ���Ʊ�K2FeO4�ij��÷��������֣�
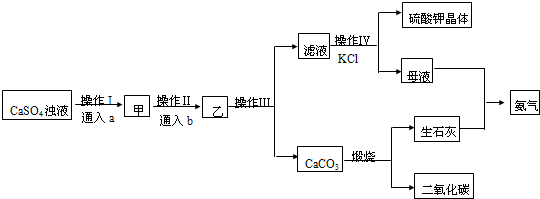
����һ��ʪ��������������ͼ1��

��1����ɡ������������з�Ӧ�Ļ�ѧ����ʽ��
2FeCl3+10NaOH+3NaClO�T2Na2FeO4+9NaCl+5H2O��������������NaClO���ѧʽ����
��2�����뱥��KOH��Һ��Ŀ���Ǽ�С������ص��ܽ⣬�ٽ�������ؾ����������������ϴ�ӵ�Ŀ����ϴȥ������ؾ�������KOH���������ʣ��õ�����Ʒ������أ�
���������ɷ�����Fe2O3��KNO3��KOH��ϼ��������Ϻ�ɫ�������κ�KNO2�Ȳ��
��3���ڸɷ��Ʊ�K2FeO4�ķ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ3��1��
������ز�����һ�������ˮ�����������Ҹ�����ص�����Ҳ�ڽ����У���ͼ2�Ǹ�����ص�ʵ��װ�ã�
��֪�ŵ�������õ�������ͬ��̬�Ļ����
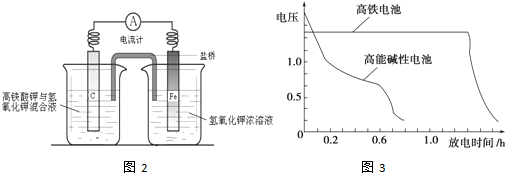
��4���õ�طŵ�ʱ���������ĵ缫��Ӧ��FeO42-+4H2O+3e-=Fe��OH��3��+5OH-��
��5�����õ�����ڶ��ε�أ�����ʱ������Ӧ�ĵ缫��Ӧ����ʽΪ��Fe��OH��3+3e-=Fe+3OH-����FeOOH+3e-+H2O=Fe+3OH-����
��6����֪�����к��б���KCl��Һ���ŵ�ʱ�����ŵ��������γɱպϵ�·���������������ӵ����з����ǣ���ص��ҳأ�����ij�ָ߷��Ӳ����Ƴɸ�Ĥ�������ţ��ø�Ĥ����ͨ����������K+��H+��
��7����ͼ3Ϊ������ص�غͳ��õĸ��ܼ��Ե�صķŵ����ߣ��ɴ˿ɵó�������ص��ŵ���ʹ��ʱ�䳤��������ѹ�ȶ���
���� ����һ��ʪ��Ϊ�����������������������̣��Ȼ�����Һ�м���������ƺ��������ƣ���ӦΪ��2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O����Na2FeO4�ֲ�Ʒ��40%KOH��Һ���ܽ⣬���˳�ȥ����NaCl�����뱥��KOH��Һ��Na2FeO4ת��Ϊ�ܽ�ȸ�С��K2FeO4����Ӧ����ʽΪNa2FeO4+2KOH=K2FeO4+2NaOH����ȴ�ᾧ�����ˣ��������������ˮ��������������������������ˮϴ�Ӳ�Ʒ���Լ��ٸ�����ص���ģ�ͬʱϴȥ������ؾ�������KOH���������ʣ��õ�����Ʒ������أ�
��1����Ӧ��NaClO������������ԭ������NaCl������Ԫ���غ㣬��֪��Ӧʽ����Ҫ����NaCl��H2O�����ݻ��ϼ���������ƽ����ʽ��
��2�����뱥��KOH��Һ��������K+��Ũ�ȣ�ʹƽ�������ƶ��������������ϴȥ������ؾ�������KOH���������ʣ��õ�����Ʒ������أ�
���������ɷ���
��3�����ݺ�Ԫ�ػ��ϼ����ߵ�����Ϊ��ԭ������Ԫ�ػ��ϼ۽��͵�����Ϊ�������������û�ѧ��Ӧ����ʽ�еĻ�ѧ�������������������뻹ԭ�������ʵ���֮�ȣ�
���ݵ��װ�ã�Fe�������ŵ磬�����ϸ�����ط�����ԭ��Ӧ����������ͬ��̬�Ļ����������ص������Ժ�ǿ���ܹ�������������
��4��FeO42-�������õ�������Fe3+��
��5�����ʱFe��OH��3�������õ�������Fe��
��6�����ſ���ƽ���ɣ����ɱպϻ�·�����ã��ŵ�ʱ����������������ص��ҳأ���ij�ָ߷��Ӳ����Ƴɸ�Ĥ�������ţ��ø�Ĥֻ����ͨ����������K+��H+��
��7��ͼ3Ϊ������غͳ��õĸ��ܼ��Ե�صķŵ����ߣ����ѿ���������ص��ŵ�Ϊʹ��ʱ��ȸ��ܼ��Ե�صij����ҷŵ��ѹ�ȸ��ܼ��Ե�ص��ȶ���
��� �⣺����һ��ʪ��
��1����Ӧ��FeCl3��Na2FeO4����Ԫ�ػ��ϼ���+3������Ϊ+6�ۣ����ϼ�������3�ۣ�NaClO��NaCl����Ԫ�ػ��ϼ���+1����Ϊ-1�ۣ����ϼ��ܹ�����2�ۣ����ϼ�������С������Ϊ6����FeCl3ϵ��Ϊ2��NaClOϵ��Ϊ3������Ԫ���غ��֪ Na2FeO4ϵ��Ϊ2������Ԫ���غ��֪NaClϵ��Ϊ2��3+3=9��������Ԫ���غ��֪NaOHϵ��Ϊ9+2��2=13������Ԫ���غ��֪H2Oϵ��Ϊ5����ƽ����ʽΪ2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O��
��Ӧ��NaClO��NaCl����Ԫ�ػ��ϼ���+1����Ϊ-1�ۣ�NaClO������������ԭ������NaCl��
�ʴ�Ϊ��2��10��3��2��9NaCl��5H2O��NaClO��
��2��Na2FeO4+2KOH?K2FeO4+2NaOH�����뱥��KOH��Һ��������K+��Ũ�ȣ�ʹƽ�������ƶ����������壬�������������ˮ��������������������������ˮϴ�Ӳ�Ʒ���Լ��ٸ�����ص���ģ�ͬʱϴȥ������ؾ�������KOH���������ʣ��õ�����Ʒ������أ�
�ʴ�Ϊ����С������ص��ܽ⣬�ٽ�������ؾ���������ϴȥ������ؾ�������KOH���������ʣ��õ�����Ʒ������أ�
���������ɷ���
��3��Fe2O3+3KNO3+4KOH�T2K2FeO4+3KNO2+2H2O����Ԫ�صĻ��ϼ۽��ͣ���Ԫ�صĻ��ϼ����ߣ���KNO3Ϊ��������Fe2O3Ϊ��ԭ�����������뻹ԭ�������ʵ���֮��Ϊ3��1��
�ʴ�Ϊ��3��1��
��4��FeO42-�������õ�������Fe3+��������缫��ӦʽΪ��FeO42-+4H2O+3e-�TFe��OH��3��+5OH-��
�ʴ�Ϊ��FeO42-+4H2O+3e-�TFe��OH��3��+5OH-��
��5�����ʱFe��OH��3�������õ�������Fe����缫��ӦʽΪ��Fe��OH��3+3e-=Fe+3OH-����FeOOH+3e-+H2O=Fe+3OH-����
�ʴ�Ϊ��Fe��OH��3+3e-=Fe+3OH-����FeOOH+3e-+H2O=Fe+3OH-����
��6�������������������ƶ����������������ʹ������������һ��ͨ·��ʹ����Һ���ֵ����ԣ���ƽ���ɣ����ɱպϻ�·���ŵ�ʱ����������������ص��ҳأ���ij�ָ߷��Ӳ����Ƴɸ�Ĥ�������ţ��ø�Ĥֻ����ͨ����������K+��H+��
�ʴ�Ϊ���γɱպϵ�·����ص��ҳأ�K+��H+��
��7��ͼ3Ϊ������غͳ��õĸ��ܼ��Ե�صķŵ����ߣ��ɴ˿ɵó��ĸ�����ص��ŵ��зŵ�ʱ�䳤��������ѹ�ȶ����ŵ㣬
�ʴ�Ϊ��ʹ��ʱ�䳤��������ѹ�ȶ���
���� ���⿼���˹�ҵ���Ʊ�K2FeO4�ij��÷��������ؿ��������Ʊ������ķ���Ӧ�ã����̵�����Ӧ�ã������������ʺ�ƽ���ƶ�ԭ���������ܽ�ȵĴ�С�Ƚ��Լ���ѧ��ع���ԭ���ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | x=y+0.2 | B�� | x=$\frac{y}{2}$ | C�� | x=0.1+$\frac{y}{2}$ | D�� | x=y |
| ҩƷ���� | �۵�/�� | �е�/�� | �ܶ�g/cm3 | �ܽ��� |
| ������ ��CH3CH2CH2OH�� | -89.5 | 117.7 | 0.8098 | ����ˮ������Ũ���� |
| l-�嶡�� ��CH3CH2CH2CH2Br�� | -112.4 | 101.6 | 1.2760 | ������ˮ��Ũ���� |
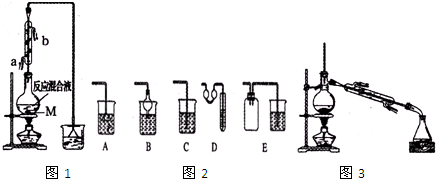
��1����Ӧװ���л���Ҫ���˹���M������M��Ŀ���Ƿ�ֹҺ�屩�У������������Ϊ1��1���������õIJ�������Ϊbcd��a����ƽ��b����Ͳ�� C����������d���ձ�
��2�������ܵĽ�ˮ���ǣ��ˣ�����ѡ���ԭ�����ܸ����������
��3������ͼ2װ���У��ܴ���ͼ1�������ռ�װ�����B��D��E��
��4������Ũ�������ʵ�飬�л����л�����ػ�ɫ����ȥ�������ʵ���ȷ������d
a��������������b������������Һϴ��
c�����ķջ�̼��ȡ d��������������Һϴ��
��5���Ʊ���Ʒ�����õ��Ĵ�1һ�Ķ���������Ũ���ᡢˮ��10д̼���ơ�ˮϴ�Ӻ������ˮץ���ƽ��и��Ȼ���ٽ�1-�Ķ��鰴ͼ3װ������
���ռ���Ʒʱ�����Ƶ��¶�Ӧ��101.6�����ң�����1һ�Ķ��龫Ʒ�ʹ�Ʒ��һ�ַ����Dz��۷е㣮
��ʵ���Ƶõ�1һ�Ķ��������Ϊ10.895g������������ת����Ϊ72.6%��������3λС����
| A�� | Na2SO3��Һ��Ba��OH��2��Һ�� | B�� | FeCl2��Һ��KSCN��Һ�� | ||
| C�� | KI��������Һ�� | D�� | NaOH��Һ��Ba��OH��2��Һ�� |
| A�� | ����Ԫ�غͷǽ���Ԫ�طֽ��߸�����Ԫ�� | |
| B�� | ϡ������Ԫ�� | |
| C�� | ���·�����Ľ���Ԫ�� | |
| D�� | ���Ϸ�����ķǽ���Ԫ�� |
 ��ͼ��ʾװ����ϴ������������;����ҽԺ������������ʱ��Ҳ���������Ƶ�װ�ã�����װ����ʢ�Ŵ�Լ��ƿ����ˮ������˵������ȷ���ǣ�������
��ͼ��ʾװ����ϴ������������;����ҽԺ������������ʱ��Ҳ���������Ƶ�װ�ã�����װ����ʢ�Ŵ�Լ��ƿ����ˮ������˵������ȷ���ǣ�������| A�� | ����B���ӹ��������ĸ�ƿ | |
| B�� | ����B���Ӳ������������ܽ��� | |
| C�� | ��װ�ÿ���������������װ���г�������ˮ�������ӵ���Bͨ�� | |
| D�� | ��װ�ÿ������۲�Ӷ���������������ٶ� |