题目内容
在一密闭容器中进行以下可逆反应:M(g) + N(g)  P(g) + 2L。在不同的条件下P的百分含量P%的变化情况如图,则反应
P(g) + 2L。在不同的条件下P的百分含量P%的变化情况如图,则反应
| A.正反应放热,L是固体 | B.正反应放热,L是气体 |
| C.正反应吸热,L是气体 | D.正反应放热,L是固体或气体 |
B
解析试题分析:对比图像中Ⅰ、Ⅱ,同压强,不同温度,温度越高,P的百分含量P%越低,所以正反应放热;对比Ⅱ、Ⅲ同温度,不同压强,压强越大,P的百分含量P%越低,L是气体。所以答案B正确。
考点:化学反应限度的图像问题。

练习册系列答案
相关题目
一定条件下,C0与H2反应可生成乙醇:2CO+4H2? CH3CH20H+H20。下列关于该反应的说法错误的是
| A.增大CO的浓度能减小反应速率 |
| B.升高体系温度能增大反应速率 |
| C.使用合适的催化剂可增大反应速率 |
| D.若反应在密闭容器中进行,H2和C0不能全部转化为产物 |
在容积一定的密闭容器中发生可逆反应:A(g)+2B(g) 2C(g) ΔH>0,其他条件不变化,只有温度变化时,某量随温度变化的关系如图所示。则下列说法中,正确的是
2C(g) ΔH>0,其他条件不变化,只有温度变化时,某量随温度变化的关系如图所示。则下列说法中,正确的是
| A.若P1>P2,纵坐标表示A的质量分数 |
| B.若P1<P2,纵坐标表示C的质量分数 |
| C.若P1>P2,纵坐标表示混合气体的平均摩尔质量 |
| D.若P1<P2,纵坐标表示A的转化率 |
重铬酸钾溶液中存在如下平衡:Cr2O72-(橙红色)+H2O  2H++2CrO42-(黄色),向K2Cr2O7溶液中加入下列哪种试剂,溶液颜色会从黄色逐渐变为橙红色
2H++2CrO42-(黄色),向K2Cr2O7溶液中加入下列哪种试剂,溶液颜色会从黄色逐渐变为橙红色
| A.NaHSO4 | B.NaHCO3 | C.Na2CO3 | D.CH3COONa |
在密闭容器中存在下列平衡:CO(g)+H2O(g)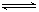 CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是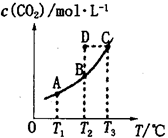
| A.平衡状态A与C相比,平衡状态A的c(CO)小 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
C.反应CO(g)+H2O(g)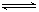 CO2(g)+H2(g)△H>0 CO2(g)+H2(g)△H>0 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
在下列影响化学反应速率的因素中,肯定能使化学反应速率加快的是( )
①升高温度②使用适宜的催化剂③增大反应物的浓度④将固体快状反应物磨成粉末⑤增大压强
| A.①②③⑤ | B.①②④⑤ | C.①③④⑤ | D.①②③④ |
 xC(g) △H<0测得两容器中c(A)随时间t的变化如图所示。
xC(g) △H<0测得两容器中c(A)随时间t的变化如图所示。
 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是 3 C(g)达到平衡时,测得c(A)=0.5 mol/L。在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L。下列判断中正确的是
3 C(g)达到平衡时,测得c(A)=0.5 mol/L。在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L。下列判断中正确的是