题目内容
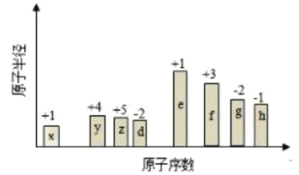
【题目】随原子序数的递增,八种短周期元素的原子半径的相对大小、最高正价或最低负价的变化如下图所示,下列分析正确的是( )
A.![]() 、
、![]() 的简单离子半径大小:
的简单离子半径大小:![]()
B.元素的金属性:![]()
C.元素的非金属性:![]()
D.![]() 、
、![]() 、
、![]() 和
和![]() 四种元素能形成离子化合物
四种元素能形成离子化合物
【答案】D
【解析】
从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素,结合元素周期律分析解答。
A.d为O、e为Na,两种离子具有相同电子层排布,原子序数大的离子半径小,则简单离子半径大小:d>e,故A错误;
B.e为Na、f为Al,同周期元素,从左向右,金属性减弱,则元素的金属性:e>f,故B错误;
C.d为O、g为S,同主族元素,从上到下,非金属性减弱,则元素的非金属性:d>g,故C错误;
D.x、y、z 和 d 四种元素可以形成碳酸铵、碳酸氢铵,均为离子化合物,故D正确;
故选D。

练习册系列答案
相关题目